1. O documento discute o tema da corrosão metálica em um curso de Química Tecnológica.
2. Apresenta conceitos básicos sobre corrosão como um processo eletroquímico de oxidação-redução.
3. Fornece detalhes sobre números de oxidação e como determiná-los em diferentes compostos químicos.









![10
UFSC – EMB5006 – Química Tecnológica – Corrosão Metálica
Corrosão
Metálica
Qual o NOX do enxofre nestes dois compostos?
H2SO3 e H2SO4
Ex.: H2SO3 → 2(1+) + X + 3(2-) = 0
2 + X - 6 = 0
X = + 6 - 2 X = 4+
H2SO4 → 2(1+) + X + 4(2-) = 0
2 + X - 8 = 0
X = + 8 - 2 X = 6+
E nestes dois: HNO3 e HNO2?
19
Determinação do Nox
2-
1+ X
2-
1+ X
Corrosão
Metálica
Fe
H2O
H2O2
HCl
HClO4
HClO
HNO3
H2SO3
H2SO4
H3PO4
K2Cr2O7
K3[Fe(CN)6]
K4[Fe(CN)6]
Cu(SO4).5H2O
(SO4)2-
(NO3)1-
(PO4)3-
[Fe(CN)6]3-
20
Números de Oxidação - Nox](https://image.slidesharecdn.com/ufsc-emb5006-corrosometlicaparte011-220619164358-54a631e2/85/UFSC-EMB5006-Corrosao-Metalica-Parte-01-1-pdf-10-320.jpg)





![16
UFSC – EMB5006 – Química Tecnológica – Corrosão Metálica
Corrosão
Metálica
Potencial do eletrodo padrão (Eo):
É a diferença de potencial (em Volts) entre o
elemento e uma solução 1M de seus íons em
relação ao eletrodo padrão de H2
E: difícil de medir sem uma referência
Eletrodo padrão de H2: é um eletrodo utilizado para a
medição do E de um metal:
Constrói-se uma pilha com H2 e o metal
Considera-se o E do H2 como “zero” e a ddp formada pela
pilha será o Eo do metal
31
Potencial de Eletrodo
Corrosão
Metálica
Por ex.: formada uma pilha entre uma barra de Zn
imerso em ZnSO4 [1M] ligada a uma pilha padrão de
H2 inserido em uma solução ácida (H+) [1M]
32
Potencial de Eletrodo](https://image.slidesharecdn.com/ufsc-emb5006-corrosometlicaparte011-220619164358-54a631e2/85/UFSC-EMB5006-Corrosao-Metalica-Parte-01-1-pdf-16-320.jpg)







![26
UFSC – EMB5006 – Química Tecnológica – Corrosão Metálica
Corrosão
Metálica
Onde:
E = potencial real [Volt]
E0 = potencial padrão [Volt]
R = cte dos gases ideais
8,314 [J/K.mol]
T = temperatura [K]
n = número de elétrons
(modificação do NOX ou
número de elétrons
ganhos pelo oxidante)
F = cte de Faraday = 96500
Coulombs
a = atividade do estado
reduzido e atividade do
estado oxidado
Sendo: ln = 2,303 log
Equação de Nernst
51
, .
, !
" #$. %&'
" #$. ()*
%
+
" #$. %&'
" #$. ()*
Corrosão
Metálica
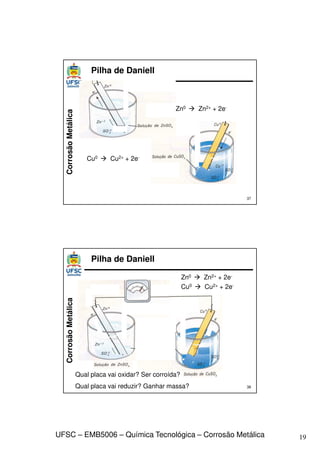
Equação de Nernst – Casos:
52
Assim, para 25 oC e 1 atm:
Para soluções muito diluídas,
, . ,
, !
" #$. %&'
" #$. ()*
,
!
" #$. %&'
" #$. ()*
,
!
,-./
Para 25 oC 298,15 K:
Para soluções com concentração 1 M
,
! →](https://image.slidesharecdn.com/ufsc-emb5006-corrosometlicaparte011-220619164358-54a631e2/85/UFSC-EMB5006-Corrosao-Metalica-Parte-01-1-pdf-26-320.jpg)
![27
UFSC – EMB5006 – Química Tecnológica – Corrosão Metálica
Corrosão
Metálica
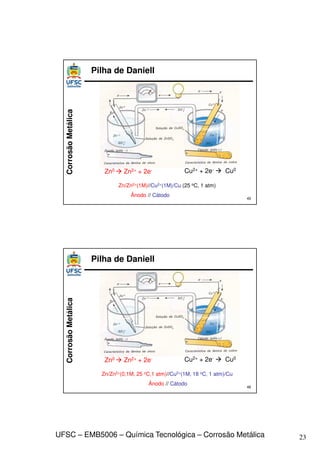
n tabela Cu2+ + 2e Cu0 n = 2
Exercício:
Usando a equação de Nernst determine o potencial do
eletrodo de Cu imerso em uma solução 0,01 M (muito
diluída) de Cu2+ a T= 30 oC?
[M+] = 0,01 M
Equação de Nernst
E0 tabela (potencial de redução) 0,337 V
53
, 1
, !
,2./
T = 30 oC = 30 +273,15 = 303,15 K
Corrosão
Metálica
n = 2
Exercício:
Usando a equação de Nernst determine o potencial do
eletrodo de Cu imerso em uma solução 0,01 M (muito
diluída) de Cu2+ a T= 30 oC?
T = 303,15 K
[M+] = 0,01 M
Equação de Nernst
E0 = + 0,337 V
54
, 1
, !
,2./
,
, ,
, !
,
, , ! 3
, , .
,](https://image.slidesharecdn.com/ufsc-emb5006-corrosometlicaparte011-220619164358-54a631e2/85/UFSC-EMB5006-Corrosao-Metalica-Parte-01-1-pdf-27-320.jpg)

![29
UFSC – EMB5006 – Química Tecnológica – Corrosão Metálica
Corrosão
Metálica
Assim: Exemplo:
Zn2+
(aq) + Cu(s) Zn(s) + Cu2+
(aq)
com:
Ecel = +1,10 V
Calculando a espontaneidade:
ΔGo = -n F Δ Eo = -2 mol . 96485 J.V-1.mol-1
* 1,10 V
ΔGo = - 212,267 kJ/mol reação espontânea
Espontaneidade das Reações
57
Corrosão
Metálica
Mg2+ + 2e- Mg E0
red = -2,370 V
Al3+ + 3e- Al E0
red = -1,660 V
Ti2+ + 2e- Ti E0
red = -1,630 V
Mn2+ + 2e- Mn E0
red = -1,180 V
Zn2+ + 2e- Zn E0
red = -0,763 V
Fe2+ + 2e- Fe E0
red = -0,440 V
Cd2+ + 2e- Cd E0
red = -0,403 V
Ni2+ + 2e- Ni E0
red = -0,250 V
58
Potencial de Eletrodo – Lista
ΔGo = -n F ΔEo
F = 96500 C
Sn2+ + 2e- Sn E0
red = -0,136 V
Pb2+ + 2e- Pb E0
red = -0,126 V
2H+ + 2e- H2 E0
red = -0,000 V
Cu2+ + 2e- Cu E0
red = +0,337 V
Cu+ + 1e- Cu E0
red = +0,521 V
Ag+ + e- Ag E0
red = +0,799 V
Au3+ + 3e- Au E0
red = +1,500 V
[ ]
+
= −
0 8 314 1
2 303
96500
, T
E E , log
n M](https://image.slidesharecdn.com/ufsc-emb5006-corrosometlicaparte011-220619164358-54a631e2/85/UFSC-EMB5006-Corrosao-Metalica-Parte-01-1-pdf-29-320.jpg)