As principais diferenças entre tumor maligno (câncer) e tumor benigno são:
Tumor maligno (câncer):
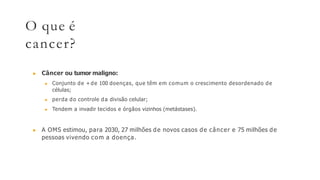
- Pode invadir tecidos e órgãos vizinhos através de metástases.
- Tem potencial para se espalhar para outras partes do corpo.
- Em geral, causa mais danos ao organismo e pode levar à morte se não tratado.
Tumor benigno:
- Não invade tecidos vizinhos nem se espalha para outras partes do corpo através de metástases.
- Embora possa