Tabela periodica
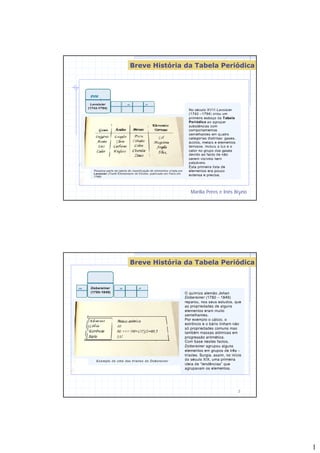
- 1. 1 Breve História da Tabela Periódica Marília Peres e Inês Bruno1 Breve História da Tabela Periódica 2
- 2. 2 Breve História da Tabela Periódica 3 Breve História da Tabela Periódica 4
- 3. 3 5 Breve História da Tabela Periódica 6
- 4. 4 Consulta: http://www.ptable.com/ 7 Período Os elementos estão colocados horizontalmente, em sequência numérica, de acordo com seus números atómicos; Cada período, à excepção do primeiro, começa com um metal e termina com um gás nobre. Sete linhas horizontais - PERÍODOSPERÍODOS. N.ºN.º dodo PERÍODO =PERÍODO = valorvalor dodo n.ºn.º quânticoquântico principalprincipal dasdas orbitaisorbitais dede valênciavalência. 8
- 5. 5 → São formados por linhas verticais; → Os elementos de cada coluna – grupo - possuem igual número de electrões de valência, responsáveis pela semelhança de propriedades químicas que esses elementos apresentam; GrupoGrupo → Os elementos do mesmo grupo constituem uma “família” . → O hidrogénio, atendendo às suas características, não pertence a nenhum grupo) N.º do GRUPO = n.º de electrões de valênciaN.º do GRUPO = n.º de electrões de valência Excepções: He e os elementos que pertencem ao 2º e 3º períodos com orbitais de valência do tipo p → n.º grupo = n.º de electrões de valência + 109 GRUPO 1 ‐ METAIS ALCALINOS → o sódio e o potássio aparecem com abundância na Natureza; → o lítio, o rubídio e o césio são mais raros; → configuração electrónica da camada de valência: o t o, o ub d o e o cés o são a s a os; Propriedades Físicas: ◊ sólidos à temperatura ambiente; ◊ moles e maleáveis; nsns11 ◊ moles e maleáveis; ◊ excelentes condutores do calor e da electricidade. 10
- 6. 6 GRUPO 1 ‐ METAIS ALCALINOS Propriedades Químicas: ◊ não se encontram livres na natureza devido à sua◊ não se encontram livres na natureza devido à sua extrema reactividade; ◊ Expostos ao ar oxidam‐se rapidamente (só as superfícies recém‐formadas apresentam brilho metálico); ◊ Têm que se guardar ao abrigo do ar, em petróleo ou tolueno ou numa atmosfera inerte; ◊ reagem com a água formando hidróxidos – MOH. 11 GRUPO 2GRUPO 2 METAIS ALCALINOMETAIS ALCALINO--TERROSOSTERROSOS → configuração electrónica da camada de valência: . nsns22 ◊ sólidos à temperatura ambiente; ◊ moles e maleáveis mas menos que os elementos do grupo 1; Propriedades Físicas: ◊ excelentes condutores do calor e da electricidade. 12
- 7. 7 GRUPO 2GRUPO 2 METAIS ALCALINOMETAIS ALCALINO--TERROSOSTERROSOS Propriedades Químicas:Propriedades Químicas: ◊ Não se encontram livres na natureza devido à sua extrema reactividade (inferior à dos elementos do grupo 1); ◊ Expostos ao ar oxidam‐se rapidamente (só as superfícies recém‐formadas apresentam brilho metálico); ◊ reagem com a água formando hidróxidos – M(OH)2 . 13 MetaisMetais dede TransiçãoTransição (grupo 3 ao 12) A parte central da tabela periódica, é uma ponte entre os elementos do bloco ss (grupos 1 e 2) e os elementos do bloco pp (grupos 13 ao 18). Os elementos preenchem o subnível d - "elementos do bloco dd ";; Todos estes elementos preenchem o subnível f - "elementos do bloco ff “. 14
- 8. 8 MetalóidesMetalóides ou Semiou Semi--MetaisMetais → separa os elementos à direita em não‐metálicos, e à esquerda em metálicos; → apresentam propriedades de metais e de não‐metais. 15 Grupo 13Grupo 13 -- Família do BoroFamília do Boro nsns22 npnp11 configuração electrónica da camada de valência G 14G 14 F íli d C bF íli d C b configuração electrónica da camada de valência Grupo 15Grupo 15 -- Família do AzotoFamília do Azoto nsns22 npnp22 Grupo 14Grupo 14 -- Família do CarbonoFamília do Carbono configuração electrónica nsns22 npnp33 Grupo 16Grupo 16 -- Família do OxigénioFamília do Oxigénio configuração electrónica da camada de valência g ç da camada de valência pp nsns22 npnp44 16
- 9. 9 GRUPO 17 GRUPO 17 ‐‐ HALOGÉNEOSHALOGÉNEOS ‐ São designados por halogéneos, nome que significa geradores de sais; fi ã l t ó i d lê i nsns22 npnp55 → Dotados de grande reactividade química (reagem com os elementos do grupo 1 formando sais chamados halogenetos; ‐ configuração electrónica de valência: nsns22 npnp55 Propriedades Químicas: Não existem livres na Natureza (tendem a formar moléculas diatómicas). g p g ; 17 GRUPO 18 GRUPO 18 ‐‐ GASESGASES RAROSRAROS → Existem na atmosfera, como gases não combinados (os átomos encontram se isolados sem se ligarem uns aos(os átomos encontram‐se isolados, sem se ligarem uns aos outros); → Têm a camada externa totalmente preenchida de electrões, o que os torna elementos quimicamente inertes; → configuração electrónica de valência: .nsns22 npnp66 18
- 10. 10 CCAUSASAUSAS DADA VARIAÇÃOVARIAÇÃO PERIÓDICAPERIÓDICA DASDAS PROPRIEDADESPROPRIEDADES DOSDOS ELEMENTOSELEMENTOS AOAO LONGOLONGO DADA TTABELAABELA PPERIÓDICAERIÓDICA:: Efeito do aumento do número quântico principal (n), das orbitaisEfeito do aumento do número quântico principal (n), das orbitais de valência;de valência; (os electrões de valência são mais energéticos, ficam mais afastados do núcleo e menos atraídos por este) Efeito do aumento da carga nuclearEfeito do aumento da carga nuclear; (os electrões sofrem um aumento da atracção por parte do núcleo(os electrões sofrem um aumento da atracção por parte do núcleo, conduzindo à contracção da nuvem electrónica) Efeito do aumento do número de electrõesEfeito do aumento do número de electrões; (há uma maior repulsão entre os electrões conduzindo à expansão da nuvem electrónica) 19 AoAo longolongo dodo grupogrupo aumenta o número quântico principal, a carga nuclear e o número de electrões, mas o efeitoefeito predominantepredominante é, em geral, oo aumentoaumento dodo númeronúmero quânticoquântico principalprincipal. AoAo longolongo dodo períodoperíodo aumenta a carga nuclear e o ú õ énúmero de electrões, mas o efeitoefeito predominantepredominante é, em geral, oo aumentoaumento dada cargacarga nuclearnuclear. 20
- 11. 11 Elemento metálicoElemento metálico - o raio atómico é metade da distância média entre os dois núcleos de dois átomos metálicos adjacentes. RAIORAIO ATÓMICOATÓMICO Elemento nãoElemento não -- metálicometálico - o raio atómico é designado como raio covalente do elemento e é metade da distância média entre os núcleos dos dois átomos ligados por uma ligação covalente. 21 Aumenta o número quântico principal Variação do raio atómicoVariação do raio atómico AOAO longo dolongo do grupogrupo Os electrões de valência ocupam níveis de energia p g sucessivamente superiores Existe um maior afastamento dos electrões de valência ao núcleo Aumento da nuvem electrónica O raio atómicoO raio atómico aumentaaumenta ao longo do grupo.ao longo do grupo. Maior tamanho do átomo. Aumento da nuvem electrónica 22
- 12. 12 Os elementos apresentam igual n.º de níveis de energia ocupados Variação do raio atómico ao longo doVariação do raio atómico ao longo do períodoperíodo A carga nuclear e o n.º de electrões de valência à did ó iaumenta à medida que aumenta o n.º atómico As forças de atracção núcleo – electrões de valência são mais intensas (prevalece o efeito do aumento da carga nuclear) O raio atómicoO raio atómico diminuidiminui ao longo do período.ao longo do período. Menor tamanho do átomo. Contracção da nuvem electrónica 23 VVARIAÇÃOARIAÇÃO DODO RAIORAIO ATÓMICOATÓMICO longodolongodococoaumentaaumentaaoao O raio atómicoO raio atómico diminuidiminui ao longo doao longo do períodoperíodo OraioatómicOraioatómic grupogrupo 24
- 13. 13 VVARIAÇÃOARIAÇÃO DODO RRAIOAIO AATÓMICOTÓMICO 25 RRELAÇÃOELAÇÃO ENTREENTRE OO RAIORAIO ATÓMICOATÓMICO EE IÓNICOIÓNICO Átomos de determinados elementos tendem a transformar‐se em iões, positivos ou negativos, de modo a atingirem uma estrutura electrónica estável. raioraio atómicoatómico << raioraio dodo aniãoaniãoraioraio atómicoatómico << raioraio dodo aniãoanião Embora a sua carga nuclear seja a mesma, aumenta o n.º de electrões e, i l õ l ã / l ã Se o átomo se transforma num anião, capta electrões. por isso, as repulsões electrão/electrão aumentam também, e consequentemente verifica‐se uma expansão da nuvem electrónica. 26
- 14. 14 raioraio atómicoatómico >> raioraio dodo catiãocatião Se o átomo se transforma num catião há remoção de electrões de valência. Como o catião tem menos electrões, embora a carga nuclear seja a mesma, as repulsões electrão/electrão diminuem e a força que o núcleo exerce sobre eles aumenta, provocando uma contracção da nuvem electrónica. 27 RRAIOAIO DEDE ÁTOMOSÁTOMOS EE IIÕESÕES IISOELECTRÓNICOSSOELECTRÓNICOS 28
- 15. 15 EENERGIANERGIA DEDE IIONIZAÇÃOONIZAÇÃO É a energia mínima necessária para remover umÉ a energia mínima necessária para remover um electrão do átomo na fase gasosa e no estadoelectrão do átomo na fase gasosa e no estadoelectrão do átomo na fase gasosa e no estadoelectrão do átomo na fase gasosa e no estado fundamental.fundamental. X+ (g) + e‐X (g) + energia A remoção do primeiro electrão, que é o mais afastado do núcleo, requer uma quantidade de energia denominada por primeira energia de ionização (I1) e, assim, sucessivamente. 29 Os elementos apresentam igual n.º de níveis de energia ocupados VVARIAÇÃOARIAÇÃO DADA EE DEDE IIONIZAÇÃOONIZAÇÃO AOAO LONGOLONGO DODO PERÍODOPERÍODO A carga nuclear e o n.º de electrões de valência aumenta à medida que aumenta o n.º atómico (prevalece o efeito do aumento da carga nuclear) Aumenta a força de atracção núcleo –Aumenta a força de atracção núcleo electrões de valência Aumenta a energia necessária para arrancar o electrão. A energia de ionização aumenta ao longo do período. 30
- 16. 16 Aumento do número quântico principal VVARIAÇÃOARIAÇÃO DADA EENERGIANERGIA DEDE IIONIZAÇÃOONIZAÇÃO AOAO LONGOLONGO DODO GRUPOGRUPO Os electrões de valência ocupam níveis deOs electrões de valência ocupam níveis de energia sucessivamente superiores Aumenta a distância dos electrões de valência ao núcleo Diminui a força de atracção núcleo – A energia de ionização diminui ao longo do grupo. electrões de valência Diminui a energia necessária para arrancar o electrão. 31 VVARIAÇÃOARIAÇÃO DADA EENERGIANERGIA DEDE IIONIZAÇÃOONIZAÇÃO 32
