1. O documento discute conceitos termodinâmicos relacionados a misturas, incluindo volume parcial molar, energia de Gibbs parcial molar e equação de Gibbs-Duhem.
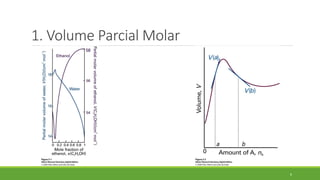
2. É explicado que o volume parcial molar representa a contribuição de um componente para o volume total da mistura.
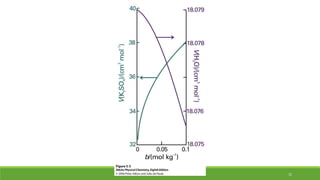
3. A energia de Gibbs parcial molar mostra como a energia de Gibbs total varia com a composição da mistura.