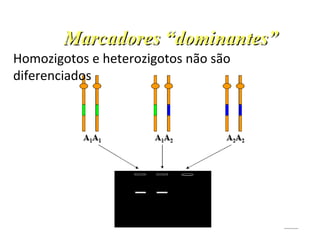
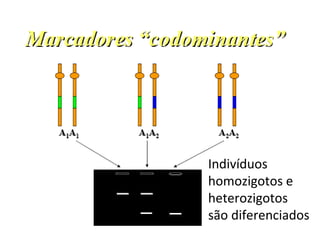
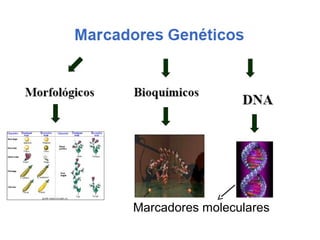
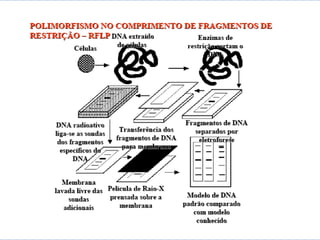
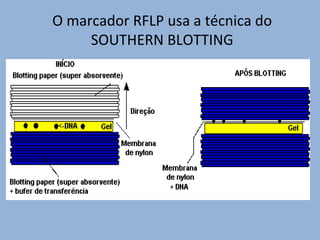
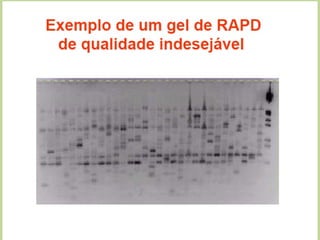
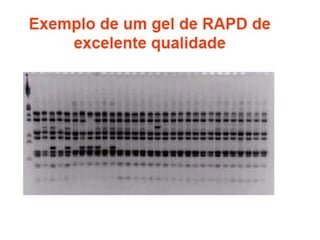
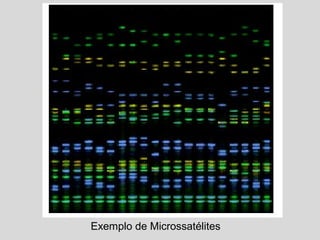
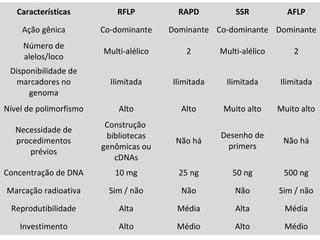
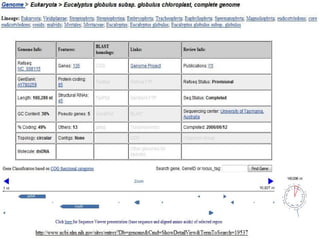
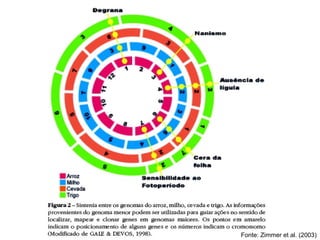
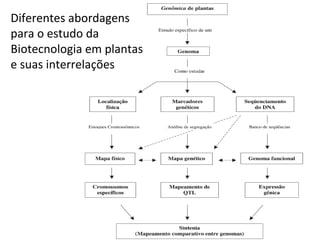
O documento discute diferentes tipos de marcadores moleculares e suas aplicações em genética e melhoramento de plantas. Aborda marcadores como RFLP, RAPD, microssatélites, AFLP e SNPs, explicando suas vantagens e desvantagens. Também apresenta informações sobre o avanço da genômica, com a sequência de genomas de diversas espécies vegetais.