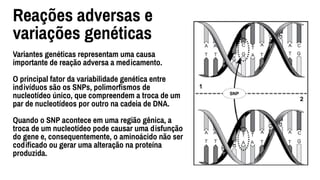
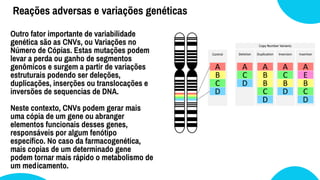
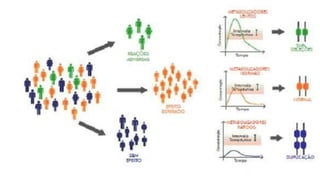
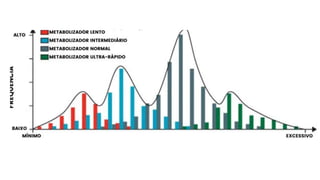
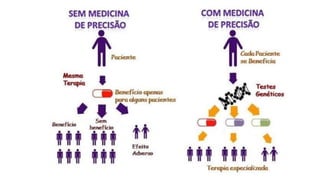
O documento discute farmacogenética, que estuda como os genes afetam a resposta a medicamentos. Apresenta os principais conceitos como perfis de metabolização, exemplos de variações genéticas que causam reações adversas, e como a farmacogenética é aplicada na medicina de precisão para personalizar tratamentos.