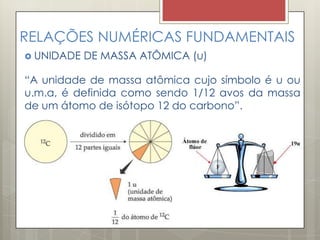
O documento discute relações numéricas fundamentais para cálculos químicos e estequiometria. Aborda conceitos como unidade de massa atômica, abundância relativa de isótopos, massa molecular, quantidade de matéria em mols, constante de Avogadro e massa molar. Apresenta também exemplos de cálculos envolvendo estas grandezas e listas de exercícios para revisão.