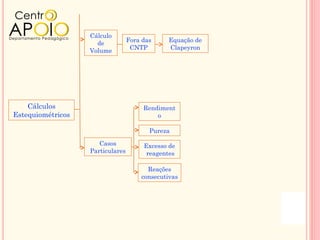
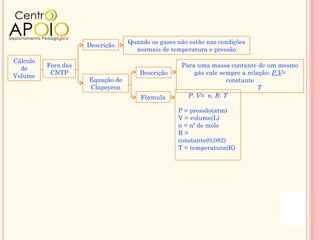
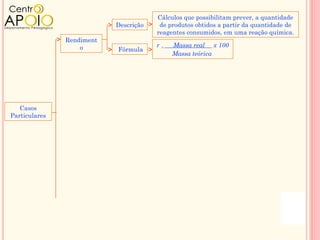
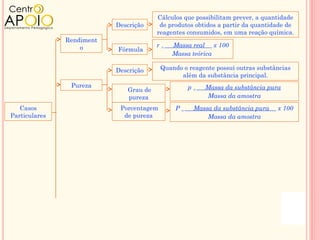
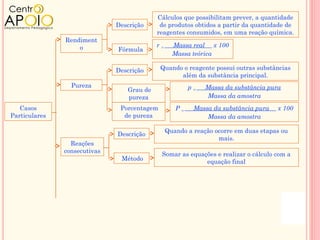
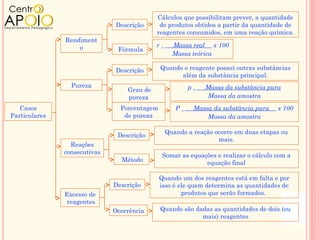
O documento discute conceitos de química relacionados à equação de Clapeyron e cálculos estequiométricos, além de abordar o rendimento de reações químicas e a pureza de substâncias. Exemplos práticos demonstram como aplicar esses princípios em problemas envolvendo gases, reações químicas e percentuais de pureza. O texto é organizado em perguntas e exercícios para prática do conhecimento adquirido.