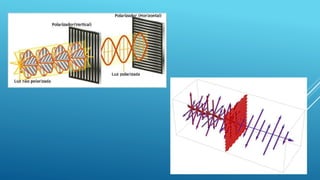
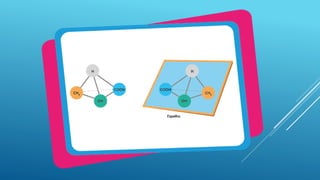
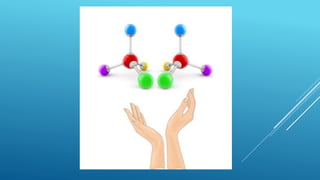
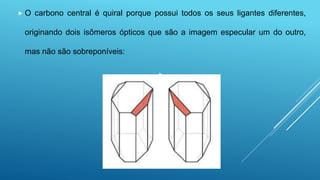
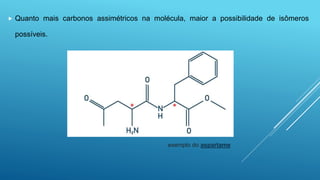
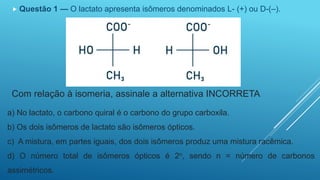
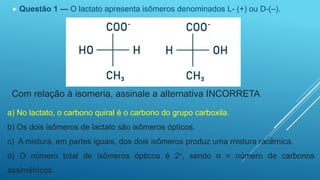
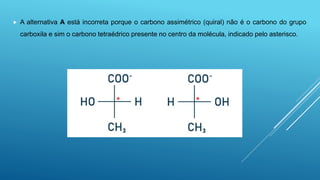
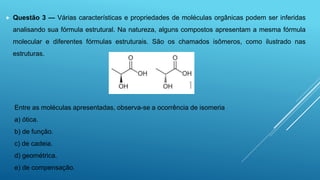
O documento discute isomeria óptica, que ocorre quando moléculas com a mesma fórmula molecular desviam a luz polarizada em sentidos opostos. Moléculas com carbonos assimétricos, que possuem quatro ligantes diferentes, podem apresentar isomeria óptica e existir como enantiômeros dextrogiros ou levogiros. O número de possíveis isômeros ópticos é calculado pela fórmula 2n, onde n é o número de carbonos assimétricos.