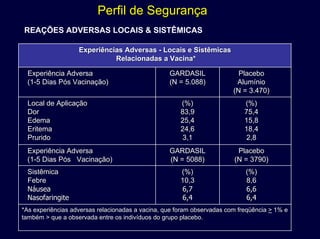
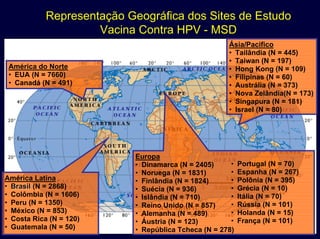
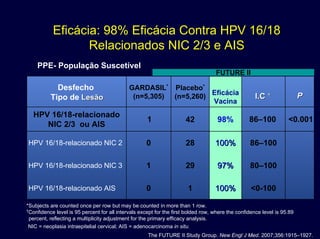
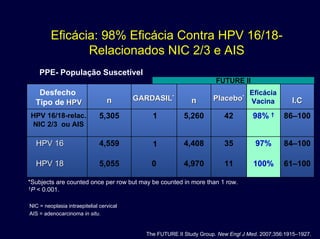
O documento discute a vacina quadrivalente contra HPV como uma ferramenta de prevenção contra câncer cervical e verrugas genitais. Apresenta dados sobre a epidemiologia dessas doenças, mecanismo de ação da vacina, eficácia e impacto esperado na redução de casos após a vacinação.












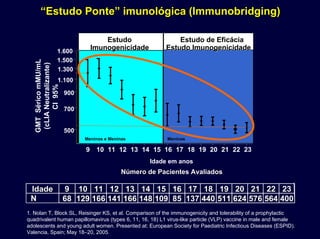

![Demonstração de Memória ImuneDemonstração de Memória Imune
Desafio de Antígeno Mês 60Desafio de Antígeno Mês 60 (007)(007)
Resposta HPV 16 * 16 - 23-anos de idade - Mulheres 5 anos de Seguimento e
evidencia de Resposta anamnéstica - Desafio imune .
0 2 6 7 1
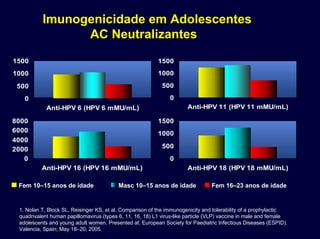
• Resultado Similar com HPV 18, 6, e 11
60+1
SemanaVacinação - Dia 0, 2 e 6 meses
Desafio Imune - Mês 60
RespostaAnti-HPVNíveisde
[Escalalog10])
10
100
1000
Gardasil N = 78
Placebo. N = 78
mMU = milli-Merck unidades
((cLiacLia –– LuminexLuminex))
Soro (-) e PCR (-)
Meses
GMT95%IC
10000 6242
3889
GARDASIL =GARDASIL =
Desafio c/Desafio c/ AgAg
Placebo =Placebo =
Dose 1Dose 1
2 24 36 54 60 61
*In subjects naïve to the relevant HPV type from day 1 through month 60
1. Data on file, MSD.](https://image.slidesharecdn.com/2vacinacomoferramentapreventiva-170524184839/85/2-vacina-como_ferramenta_preventiva-29-320.jpg)