Ácidos Carboxílicos: Estrutura, Propriedades e Reações
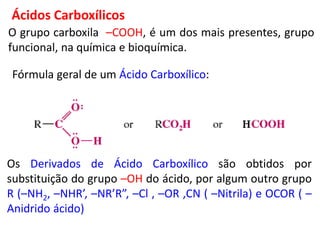
- 1. O grupo carboxila –COOH, é um dos mais presentes, grupo funcional, na química e bioquímica. Os Derivados de Ácido Carboxílico são obtidos por substituição do grupo –OH do ácido, por algum outro grupo R (–NH2, –NHR’, –NR’R”, –Cl , –OR ,CN ( –Nitrila) e OCOR ( – Anidrido ácido) Ácidos Carboxílicos Fórmula geral de um Ácido Carboxílico:
- 2. Derivados de Ácido Carboxílico
- 3. CH3CH2CHCH2CH2COH O CH3 1 2 3 4 5 6 Ácido 4-metilexanóico Ácido hex-4-enóico 6 1 2 3 4 5 CH3CH CHCH2CH2COH O HOC COH O O Ácido etanodióico CO2H NO2 Ácido 3-nitrobenzóico Nomenclatura de Ácidos Carboxílicos
- 4. ESTRUTURA NOME SISTEMÁTICO NOME COMUM HCO2H Ácido metanóico Ácido fórmico CH3CO2H Ácido etanóico Ácido acético CH3CH2CO2H Ácido propanóico Ácido propiônico CH3(CH2)2CO2H Ácido butanóico Ácido butírico CH3(CH2)3CO2H Ácido pentanóico Ácido valérico CH3(CH2)4CO2H Ácido hexanóico Ácido capróico CH3(CH2)6CO2H Ácido octanóico Ácido caprílico CH3(CH2)8CO2H Ácido decanóico Ácido cáprico CH3(CH2)10CO2H Ácido dodecanóico Ácido láurico CH3(CH2)12CO2H Ácido tetradecanóico Ácido mirístico CH3(CH2)14CO2H Ácido hexadecanóico Ácido palmítico CH3(CH2)16CO2H Ácido octadecanóico Ácido esteárico HO2C-CO2H Ácido etanodióico Ácido oxálico HO2CCH2CO2H Ácido propanodióico Ácido malônico HO2C(CH2)2CO2H Ácido butanodióico Ácido succínico
- 9. Ácidos Graxos saturados insaturados ácido mirístico 6 COOH 3 ácido linolênico (ômega-3) COOH 3 ácido linoleico (ômega-6) COOH CH3(CH2)24CO(CH2)29CH3 O componente principal da cera de abelha gordura ou óleo Ceras, Óleos e Gorduras 7 ácido palmítico COOH
- 10. A hibridização sp2 do oxigênio da hidroxila permite que um de seus pares de elétrons sejam deslocalizados por sobreposição do orbital no sistema do grupo carbonila. Em termos de ressonância, esta deslocalização do elétron é representado como: A deslocalização do par de elétrons do oxigênio hidroxila torna o grupo carbonila menos eletrofílico do que o de um aldeído ou cetona. Os ácidos carboxílicos são bastante polares, como o ácido acético, ácido propanóico e ácido benzóico apresentam momentos de dipolo num intervalo de 1,7-1,9 D. Estrutura e ligação
- 11. Os ácidos carboxílicos são substâncias polares; Suas moléculas podem formar fortes ligações de hidrogênio uma com as outras, ou com a água. Propriedades Físicas A solubilidade dos ácidos carboxílicos são semelhantes as dos álcoois. Ácidos carboxílicos de quatro átomos de carbono ou menos são miscíveis com água.
- 13. Acidez de ácidos carboxílicos Propriedades Químicas • Os ácidos carboxílicos possuem caráter ácido devido à sua ionização em água. R-COOH + H2O R-COO- + H3O+. • A força ácida pode ser maior ou menor dependendo do tipo de efeito indutivo causado pelo grupamento ligado à carboxila.
- 14. Dissociação de ácidos carboxílicos • Dissociam-se levemente em água para gerar o H3O+ e os ânions carboxilatos, RCO2 - pKa = 4,75 (para a maioria dos ácidos carboxílicos)
- 15. EFEITOS DOS SUBSTITUINTES NA ACIDEZ DOS ÁCIDOS CARBOXÍLICOS • Grupos que retiram elétron ligado à carbonila diminuem a densidade eletrônica, estabiliza o ânion carboxilato e aumenta a acidez. •Grupos que doam elétron desestabilizam o ânion carboxilato e enfraquece o ácido
- 16. EFEITOS DOS SUBSTITUINTES NOS ÁCIDOS BENZÓICOS SUBSTITUÍDOS (a) grupo NO2, retirador de elétrons, pode estabilizar o ânion carboxilato por efeito indutivo aumenta a acidez do ácido benzóico. (b) grupo CH3O é doador de elétrons (efeito oposto ao grupo NO2) diminui a acidez do ácido benzóico
- 19. Preparação de Ácidos Carboxílicos
- 20. Preparação de Ácidos Carboxílicos
- 21. Preparação de Ácidos Carboxílicos
- 22. Reações de Ácidos Carboxílicos e seus Derivados Aldeídos e Cetonas Ácidos carboxílicos e derivados
- 26. Reações de Ácidos Carboxílicos e seus Derivados Reações de Cloretos de Acila
- 27. Reações de Ácidos Carboxílicos e seus Derivados Reações de Anidridos de Ácidos Carboxílicos
- 28. Reações de Ácidos Carboxílicos e seus Derivados Reações de Ésteres
- 29. Reações de Ácidos Carboxílicos e seus Derivados Reações de Amidas
- 30. Reações de Ácidos Carboxílicos e seus Derivados Reações de Amidas
- 31. Reações de Ácidos Carboxílicos e seus Derivados Reações de Amidas
- 32. Reações de Ácidos Carboxílicos e seus Derivados Reações de Nitrilas
- 33. Reações de Ácidos Carboxílicos e seus Derivados Reações de Nitrilas