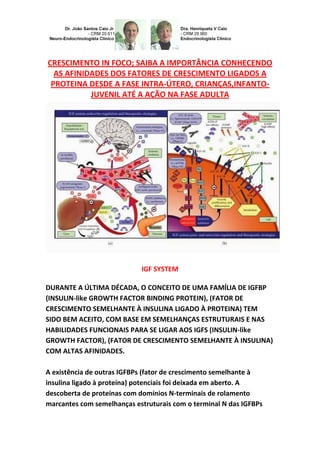
IGFBPs e crescimento: da fase fetal à vida adulta
- 1. CRESCIMENTO IN FOCO; SAIBA A IMPORTÂNCIA CONHECENDO AS AFINIDADES DOS FATORES DE CRESCIMENTO LIGADOS A PROTEINA DESDE A FASE INTRA-ÚTERO, CRIANÇAS,INFANTO- JUVENIL ATÉ A AÇÃO NA FASE ADULTA IGF SYSTEM DURANTE A ÚLTIMA DÉCADA, O CONCEITO DE UMA FAMÍLIA DE IGFBP (INSULIN-like GROWTH FACTOR BINDING PROTEIN), (FATOR DE CRESCIMENTO SEMELHANTE À INSULINA LIGADO À PROTEINA) TEM SIDO BEM ACEITO, COM BASE EM SEMELHANÇAS ESTRUTURAIS E NAS HABILIDADES FUNCIONAIS PARA SE LIGAR AOS IGFS (INSULIN-like GROWTH FACTOR), (FATOR DE CRESCIMENTO SEMELHANTE À INSULINA) COM ALTAS AFINIDADES. A existência de outras IGFBPs (fator de crescimento semelhante à insulina ligado à proteína) potenciais foi deixada em aberto. A descoberta de proteínas com domínios N-terminais de rolamento marcantes com semelhanças estruturais com o terminal N das IGFBPs
- 2. (fator de crescimento semelhante à insulina ligado à proteína) e com reduzida, mas demonstrável, afinidade para IGF (fator de crescimento semelhante à insulina), levantou a questão de saber se estas proteínas eram "novas" IGFBPs (fator de crescimento semelhante à insulina ligado à proteína). N-terminal (amino-terminal) é uma das extremidades da cadeia polipeptídica. A outra extremidade é chamada "C-terminal" ou "carboxi-terminal". Convencionou-se escrever as cadeias peptídicas da esquerda para a direita, partindo do N-terminal em direção ao C- terminal, pois é esta a sequência em que os ribossomos as sintetizam (sua principal função é sintetizar fitas proteicas de RNA (ácido ribonucleico) complementares às já existentes e produzir enzimas. As proteínas produzidas pelos polirribossomas geralmente permanecem dentro da célula para uso interno. RIBOSSOMO RETÍCULO ENDOPLASMÁTICO
- 3. Já as enzimas produzidas pelos ribossomas aderidos à parede do retículo endoplasmático são armazenadas em vesículas que são transportadas para o complexo de Golgi, onde são "empacotadas" e enviadas para fora da célula). Ao detalhar o mecanismo logístico desse transporte através de vesículas os Laureados com o Prêmio Nobel de 2013 nos deram diversos detalhes não compreendidos claramente até este ano; o Comitê dá início às premiações de 2013 laureando o trio de cientistas por trabalho que desvendou o funcionamento do mecanismo de transporte intracelular. Todos são professores de universidades americanas. Os americanos James Rothman e Randy Schekman e o alemão Thomas Südhof foram laureados com o Prêmio Nobel de Fisiologia ou Medicina de 2013, como anunciou na segunda-feira (07/10) o Instituto Karolinska em Estocolmo. Além disso, o N de ácido amino terminal de uma proteína é um fator importante que metade de suas meia-vida (probabilidade de ser degradado). Esta é a chamada regra N- end. O domínio N-terminal tinha sido associado exclusivamente com as insulin-like growth factor binding proteins (IGFBPs) e tem sido considerado como sendo críticos para a ligação de IGF, não podemos nos esquecer que o GH-hormônio de crescimento esta intimamente ligado ao IGF-1 e por consequência ao crescimento infanto juvenil e adolescentes desde a fase neonatal. Não existe nenhuma outra função confirmada para este domínio até o momento. Assim, a presença deste domínio IGFBP importante no terminal N de outras proteínas devem ser considerados significativos. Embora essas outras proteínas parecem capazes de se ligarem ao IGF, mas, a sua afinidade relativamente baixa e o fato de que suas principais ações biológicas são susceptíveis de não envolver diretamente os peptídeos insulin-like growth factor (IGF) sugerem que eles provavelmente não devem ser classificados na família das insulin-like growth factor binding protein (IGFBP) como proposto transitoriamente (ligação).
- 4. IGF/IGFBPs COMPLEX A conservação desse único domínio, tão importante para a ligação de alta afinidade de IGF pelos seis IGFBPs, em todas as IGFBP-RPS (receptores), bem, fala com sua importância biológica. Historicamente, e talvez, funcionalmente, o que levou à designação de uma "superfamília IGFBP". A classificação e nomenclatura para a superfamília IGFBP é, naturalmente, arbitrária, o que é, em última análise relevante à biologia subjacente, muito do que ainda está para ser decifrado. A nomenclatura para as proteínas relacionadas com a insulin-like growth factor binding protein (IGFBP) foi derivada a partir de um consenso dos investigadores que trabalham no campo da IGFBP. Obviamente, um consenso mais geral sobre a nomenclatura, envolvendo todos os grupos de trabalho em cada IGFBP-rP (IGFBP-rP1/mac25 é um membro recentemente descrito do fator de crescimento semelhante à insulina em proteínas (IGFBP) família vinculativa. Ele tem uma homologia estrutural com os outros membros da família de IGFBP, mas tem uma menor afinidade para fatores de crescimento semelhantes à insulina (IGFs). Em estudos anteriores usando RNA Blot de hibridação, foi demonstrado que a expressão de IGFBP-rP1/mac25 era ubíquo (unipresente) em tecidos humanos normais), ainda tem de ser alcançado. Ainda mais a
- 5. compreensão das funções biológicas de cada proteína deve ajudar a resolver o dilema da nomenclatura. Para o presente, redesignar estas proteínas IGFBP-RPS simplifica os vários nomes já associados a cada proteína IGFBP relacionadas, e reforça o conceito de uma relação com as IGFBPs. Para além do domínio N-terminal, existe uma falta de semelhança estrutural entre as IGFBP-RPS e IGFBP. Os domínios C- terminais compartilham semelhanças com outros domínios internos encontrados em inúmeras outras proteínas. Por exemplo, a semelhança entre o terminal C da IGFBP para o domínio tiroglobulina tipo I mostra que as IGFBPs são também estruturalmente relacionadas com numerosas outras proteínas que transportam o mesmo domínio. Curiosamente, as funções dos diferentes domínios C-terminais de membros da superfamília de IGFBP incluem interações com a superfície da célula ou de ECM-membrana celular externa, sugerindo que, mesmo que as pequenas semelhanças de sequência, os domínios C-terminais podem ser funcionalmente relacionados. A conservação evolutiva do domínio N-terminal e estudos funcionais suporta a noção de que a IGFBP e de IGFBP-RPS em conjunto, formam uma superfamília de IGFBP. A superfamília delineia entre proteínas intimamente relacionadas (classificada como uma família) e parentes distantes. A superfamília de IGFBP é, por conseguinte, composta por famílias distantemente relacionadas. A natureza modular dos componentes da superfamília de IGFBP, particularmente a sua conservação de um domínio N-terminal
- 6. altamente conservado, parece ser melhor explicado pelo processo de embaralhar exão de um gene ancestral que codifica este domínio (Exão ou Éxon é um segmento de DNA de um gene eucarioto cujo transcrito sobrevive ao processo de excisão. Em uma molécula de mRNA, um exão pode codificar aminoácidos de uma proteína, em outras moléculas de RNA maduro como tRNAs e rRNAs, o exão constitui parte estrutural). Ao longo do curso da evolução, alguns membros evoluiram para ligantes de IGF de alta afinidade e outros em ligantes de IGF de baixa afinidade, que confere, assim, na IGFBP superfamília a capacidade de influenciar o crescimento celular por meio tanto o IGF-dependentes e independentes. Dr. João Santos Caio Jr. Endocrinologia – Neuroendocrinologista CRM 20611 Dra. Henriqueta V. Caio Endocrinologista – Medicina Interna CRM 28930 Como Saber Mais: 1. Em uma avaliação significativa de pacientes que foram divididos em grupos de acordo com seu pico do hormônio de crescimento humano- HGH em resposta secretora a testes de estímulos e a média de concentração do hormônio de crescimento humano-HGH em um período de 24 horas... http://baixaestaturaecrescimento.blogspot.com 2. Na média de 24 horas a concentração do hormônio de crescimento humano-HGH foi significativamente maior no grupo controle do que em qualquer um dos grupos com deficiência do hormônio de crescimento humano (DNGH) clássico... http://especialistacrescimento.blogspot.com
- 7. 3. As respostas a estímulos eram intermediários para o grupo com disfunção neurossecretora de humanos (DNGH) em comparação com os que apresentavam deficiência do hormônio de crescimento humano clássica e os grupos de controles... http://baixaestaturaecrescer.blogspot.com AUTORIZADO O USO DOS DIREITOS AUTORAIS COM CITAÇÃO DOS AUTORES PROSPECTIVOS ET REFERÊNCIA BIBLIOGRÁFICA. Referências Bibliográficas: Dr. João Santos Caio Jr, Endocrinologista, Neuroendocrinologista, Dra Henriqueta Verlangieri Caio, Endocrinologista, Medicina Interna – Van Der Häägen Brazil, São Paulo, Brasil; Salmon W, Daughaday W 1957 A hormonally controlled serum factor which stimulates sulfation incorporation by cartilage in vitro. J Lab Clin Med 49:825–836; Froesch ER, Muller WA, Burgi H, Waldvogel M, Labhart A 1966 Nonsuppressible insulin-like activity of human serum. II. Biological properties of plasma extracts with nonsuppressible insulin-like activity. Biochim Biophys Acta 121:360–374; Dulak NC, Temin HM 1973 A partially purified polypeptide fraction from rat liver cell conditioned medium with multiplication-simulating activity from embryo fibroblasts. J Cell Physiol 81:153–160; Daughaday WH, Hall K, Raben MS, Salmon Jr WD, van den Brande JL, van Wyk JJ 1972 Somatomedin: proposed designation for sulphation factor. Nature 235:107; Daughaday W, Rotwein P 1989 Insulin-like growth factors I and II peptide messenger ribonucleic acid and gene structures, serum and tissue concentrations. Endocr Rev 10:68– 91; Rosenfeld R, Wilson D, Lee P, Hintz R 1986 Insulin-like growth factors I and II in the evaluation of growth retardation. J Pediatr 109:428; Rosenfeld R 1987 Somatomedin action and tissue growth-factor receptors. In: Robbins R, Melmed S (eds) Acromegaly. Plenum Press, New York, pp 45–53; Lowe L 1991 Biological actions of the insulin-like growth factors. In: LeRoith D (ed) Insulin-like Growth Factors: Molecular and Cellular Aspects. CRC Press, Boca Raton, FL, pp 49–85; Rotwein P 1991 Structure, evolution, expression and regulation of insulin-like growth factors I and II. Growth Factors 5:3–18; Jones JI, Clemmons DR 1995 Insulin-like growth factors and their binding proteins: biological actions. Endocr Rev 16:3–34. Contato: Fones: 55 11 5087-4404 ou 96197-0305 Nextel: ID:111*101625 Rua Estela, 515 - Bloco D - 12º andar - Conj. 121/122 Paraiso - São Paulo - SP - Cep 04011-002 e-mails: drcaio@vanderhaagenbrasil.com drahenriqueta@vanderhaagenbrasil.com vanderhaagen@vanderhaagenbrasil.com Site Van Der Häägen Brazil www.vanderhaagenbrazil.com.br www.clinicavanderhaagen.com.br
- 8. www.crescimentoinfoco.com www.obesidadeinfoco.com.br http://drcaiojr.site.med.br http://dracaio.site.med.br Joao Santos Caio Jr http://google.com/+JoaoSantosCaioJr google.com/+JoãoSantosCaioJrvdh google.com/+VANDERHAAGENBRAZILvdh Video http://youtu.be/woonaiFJQwY VAN DER HAAGEN BRAZI Instagram https://instagram.com/clinicascaio/ Google Maps: http://maps.google.com.br/maps/place?cid=5099901339000351730&q=Van+Der+Haagen+Brasil&hl= pt&sll=-23.578256,46.645653&sspn=0.005074,0.009645&ie =UTF8&ll=-23.575591,- 46.650481&spn=0,0&t = h&z=17
