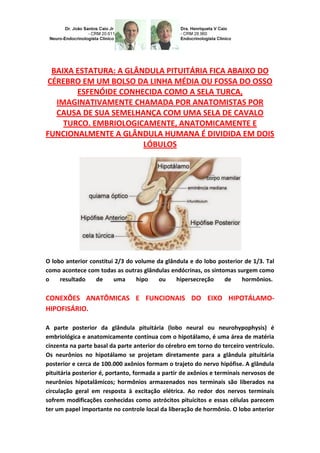
GLÂNDULA PITUITÁRIA E SUA RELAÇÃO COM O CRESCIMENTO E A BAIXA ESTATURA
- 1. BAIXA ESTATURA: A GLÂNDULA PITUITÁRIA FICA ABAIXO DO CÉREBRO EM UM BOLSO DA LINHA MÉDIA OU FOSSA DO OSSO ESFENÓIDE CONHECIDA COMO A SELA TURCA, IMAGINATIVAMENTE CHAMADA POR ANATOMISTAS POR CAUSA DE SUA SEMELHANÇA COM UMA SELA DE CAVALO TURCO. EMBRIOLOGICAMENTE, ANATOMICAMENTE E FUNCIONALMENTE A GLÂNDULA HUMANA É DIVIDIDA EM DOIS LÓBULOS O lobo anterior constitui 2/3 do volume da glândula e do lobo posterior de 1/3. Tal como acontece com todas as outras glândulas endócrinas, os sintomas surgem como o resultado de uma hipo ou hipersecreção de hormônios. CONEXÕES ANATÔMICAS E FUNCIONAIS DO EIXO HIPOTÁLAMO- HIPOFISÁRIO. A parte posterior da glândula pituitária (lobo neural ou neurohypophysis) é embriológica e anatomicamente contínua com o hipotálamo, é uma área de matéria cinzenta na parte basal da parte anterior do cérebro em torno do terceiro ventrículo. Os neurônios no hipotálamo se projetam diretamente para a glândula pituitária posterior e cerca de 100.000 axônios formam o trajeto do nervo hipófise. A glândula pituitária posterior é, portanto, formada a partir de axônios e terminais nervosos de neurônios hipotalâmicos; hormônios armazenados nos terminais são liberados na circulação geral em resposta à excitação elétrica. Ao redor dos nervos terminais sofrem modificações conhecidas como astrócitos pituicitos e essas células parecem ter um papel importante no controle local da liberação de hormônio. O lobo anterior
- 2. (ou adenohipófise) é anatomicamente distinto do hipotálamo e consiste de uma coleção de células endócrinas. Foram identificados inicialmente três tipos de células diferentes de acordo com a sua capacidade para assumir colorações histológicas gerais; estas foram denominadas cromófobas, acidófilas e basófilas. Técnicas de imunohistoquímica mais recentes permitiu a classificação das células por seus produtos específicos de secreção. Cerca de 50% das células secretoras da adeno-hipófise são somatotrófos (que sintetizam somatotrofina ou GH), 10 a 25% (lactotrófos sintetizam prolactina), 15 a 20% (corticotrófos sintetizam ACTH), 10 a 15% (gonadotrófos sintetizam gonadotrofinas LH e FSH), e 3 a 5% (tireotrófos sintetizam TSH). Algumas células, normalmente os cromófobos, não colorem com qualquer um dos anticorpos para os vários dos hormônios da pituitária anterior, embora à microscopia eletrônica revele que estas células contêm grânulos secretórios. Enquanto a glândula pituitária anterior, não seja anatomicamente relacionada com o hipotálamo, ele está funcionalmente ligado com esta parte do cérebro. As células nervosas do hipotálamo secretam neurohormônios que, através de um sistema de vasos portais hipofisários na eminência mediana, agem sobre as células endócrinas do lobo anterior para estimular ou inibir a sua síntese e secreção. Dentro do hipotálamo, existem grupos distintos de células nervosas, denominados núcleos, dispostas bilateralmente em torno do terceiro ventrículo. Aqueles que se preocupam com as secreções hormonais da glândula pituitária tendem a ser distribuídos mais medialmente enquanto aqueles preocupados com funções autônomas, como a regulação da temperatura, ingestão de alimentos, saciedade e estimulação simpática de secreções adrenomedulares, tendem a se localizar mais lateralmente. A glândula pituitária mantém suas conexões anatômicas e funcionais, com o cérebro e ainda fica fora da barreira hemato-
- 3. encefálica. A parte anterior da sela túrcica é o tubérculo da sela que é ladeado por projeções semelhantes a asas do esfenóide conhecidos como os processos crinóides anterior. A parte posterior, conhecida como o dorso da sela, é flanqueada pelos processos crinóides posterior. Estes processos crinóides são os pontos de fixação do diafragma da sela, um reflexo da dura-máter que envolve o cérebro. Desta forma, toda a glândula pituitária está rodeada por dura-máter de modo que a membrana aracnoideia e, assim, o fluido cerebrospinal, não pode entrar na sela turca. O suprimento de sangue para o eixo hipotálamo-hipofisário é complexo, mas define a relação funcional entre o hipotálamo e adenohipófise. Qualquer interrupção do fluxo de sangue prejudica o controle hipotalâmico da secreção adeno- hipofisária. O hipotálamo recebe seu suprimento de sangue a partir do polígono de Willis, enquanto a neurohipófise e a adenohipófise recebem o sangue das artérias hipofisárias inferior e superior, respectivamente. O plexo capilar dos drenos da artéria hipofisária inferior no seio dural embora alguns desses capilares na forma haste neurais veia porta "curto" que drenam para a glândula pituitária anterior. SÍNDROME DE SHEEHAN Durante a gravidez, há um aumento de aproximadamente 50% no volume da
- 4. glândula pituitária. Isto é principalmente devido à hiperplasia dos lactótrofos que secretam prolactina para preparar os seios para a lactação. Assim, enquanto o volume da pituitária aumenta a fossa em que a glândula pituitária se encontra não consegue suportar o seu crescimento. A queda súbita da pressão arterial após um evento, como uma hemorragia pós-parto causa isquemia da glândula, dano celular e edema. Por sua vez, os resultados do edema da glândula pituitária (que já é ampliada na hiperplasia dos lactótrofos) restringindo ainda mais o fluxo normal de sangue para a glândula. O resultado é um enfarte na glândula que provoca a perda das suas secreções. DEFICIÊNCIA DE CRESCIMENTO E SOMATOTROFINA Um exemplo para facilitar a compreensão: a idade é plotada no (X) eixo horizontal. Dois conjuntos de dados normais são plotados. Altura (o conjunto superior das curvas) está representada no lado esquerdo vertical (Y) e de peso (o conjunto inferior das curvas) no eixo Y à direita. Um menino, “neste caso, foi inicialmente designado por falta de prosperar”, um termo geralmente utilizado para as crianças com menos de 2 anos de idade que não estão focados em peso (ou seja, inclinar-se para a sua altura). Para interpretar este caso, é necessário entender o uso de gráficos de crescimento; a apresentação inicial estava mais perto do 3º percentil para peso e do que 3º percentil para a altura. Em outras palavras é uma criança de baixa estatura e com peso superior. Assim, ele não estava conseguindo evoluir, ele não estava conseguindo crescer. Com os pais no percentil 25, ele teria sido o esperado, todas as outras coisas sendo iguais, também o crescer ao longo dessa linha. O crescimento pós-natal nunca corresponde a esta com apenas um aumento de 20 vezes em massa e um aumento de 3 a 4 vezes em comprimento. Na infância, há um período de rápido
- 5. crescimento seguido de um período de pouco crescimento, com um retorno da aceleração do crescimento, ou melhor, um surto de crescimento puberal e uma fase de desaceleração até a altura final. O crescimento intra-uterino é regulado pelo sistema endócrino, fatores maternos e genéticos, embora os determinantes do crescimento pré-natal são pouco compreendidos. As concentrações de GH no plasma fetal são muito elevadas e ainda crianças com deficiência de GH, e mesmo aqueles com anencefalia, podem ter o comprimento normal do corpo no momento do nascimento. As influências maternas (intrauterinas) têm sido difíceis de definir, mas a má nutrição materna é o fator mais importante que leva ao baixo peso ao nascer e à duração a nível mundial. A ingestão de álcool e o tabagismo são outros fatores adversos sobre o crescimento fetal e infecções maternas, como rubéola, toxoplasmose e citomegalovírus levar a muitas alterações, bem como à baixa estatura. O GH E OS IGF: A família IGF é composta por 3 membros (insulina, IGF-1 e IGF-2) com semelhanças estruturais comuns de compartilhamento. Existem formas variantes do IGF. O IGF-1 e o IGF-2, também têm funções metabólicas, mas também desempenha um papel importante na maturação e crescimento do feto, criança, infantil e juvenil. DISABLED CHILD AND YOUTH GROWTH BY OTHER COMMITMENTS PITUITARY HORMONE ASSOCIATES.
- 6. LOW HEIGHT: THE PITUITARY GLAND IS BELOW THE BRAIN IN A POCKET OR AVERAGE LINE OF BONE FOSSA SPHENOID KNOWN AS THE TURKISH SADDLE, IMAGINATIVELY CALL FOR ANATOMISTS BECAUSE OF HIS LIKENESS WITH A SADDLE HORSE TURKISH. EMBRYOLOGICALLY, ANATOMICALLY AND FUNCTIONALLY THE GLAND IS DIVIDED INTO TWO LOBES. PHYSIOLOGY-ENDOCRINOLOGY-NEUROENDOCRINOLOGY- GENETICS-ENDOCRINE-PEDIATRICS (SUBDIVISION OF ENDOCRINOLOGY): DR. JOÃO SANTOS CAIO JR. ET DRA. HENRIQUETA VERLANGIERI CAIO. The anterior lobe is two-thirds of the volume of the gland and the posterior lobe is a third of the volume of the gland. As all other endocrine glands, symptoms arise as the result of a hypo-or hyper hormones. THE ANATOMICAL AND FUNCTIONAL CONNECTIONS OF THE HYPOTHALAMIC- PITUITARY AXIS. The posterior part of the pituitary (neurohypophysis or neural lobe) is anatomically and embryologically continuous with the hypothalamus, an area of gray matter in the basal part of the forebrain around the third ventricle. Neurons in the hypothalamus project directly to the posterior pituitary gland about 100.000 axons form the path of pituitary nerve. The posterior pituitary is thus formed from axons and nerve terminals to hypothalamic neurons; hormones stored in the terminal are released into the general circulation in response to electrical excitation. Around the nerve terminals are modified astrocytes known as pituicytes and these cells appear to play an important role in local control of hormone release. The previous (or
- 7. adenohypophysis) lobe is anatomically distinct from the hypothalamus and consists of a collection of endocrine cells. Three different cells were initially identified according to their ability to assume general histological staining; these were chromophobes, acidophils and basophils. Most recent immunohistochemical techniques enable sorting the cells by their specific secretory products. Approximately 50% of the secretory cells are anterior pituitary somatotrophs (which synthesize somatotropin or growth hormone, GH), 10 to 25% (Lactotrophs making prolactin), 15 to 20% corticotrophic hormone (ACTH), 10 to 15% gonadotrophs (LH and FSH), and 3% to 5% thyrotrophs (TSH). Some cells normally chromophobes not stain with any of the various antibodies to the hormones of the anterior pituitary, although electron microscopy reveals that these cells contain secretory granules. While the anterior pituitary gland, is not anatomically associated with the hypothalamus, it is functionally connected with this part of the brain. The nerve cells of the hypothalamus secrete neurohormones which, via a pituitary portal vasculature in the median eminence, act on the endocrine cells of the anterior lobe to stimulate or inhibit the synthesis and secretion. Within the hypothalamus, different groups of nerve cells called nuclei, bilaterally disposed around the third ventricle. Those concerned with the hormonal secretions of the pituitary gland tend to be distributed more medial while those concerned with autonomous functions such as temperature regulation, food intake and satiety and sympathetic stimulation of adrenomedullary secretions, tend to be more laterally located. The pituitary gland maintains its anatomical and functional connections with the brain still gets outside of the blood brain barrier. The anterior part of the sella is the tuber of the saddle which is flanked by wing-like sphenoid processes known as crinoid previous
- 8. projections. The back, known as the back of the saddle, is flanked by later processes crinoids. These crinoids processes are the attachment points of the diaphragm seals, a reflection of the dura mater surrounding the brain. Therefore, all of the pituitary gland is surrounded by dura so that the arachnoid membrane and thus the cerebrospinal fluid can not enter the sella turcica. The blood supply to the hypothalamic-pituitary axis is complex, but it defines the functional relationship between the hypothalamus and anterior pituitary. Any interruption of blood flow affect the hypothalamic control of pituitary adeno secretion. The hypothalamus receives its blood supply from the circle of Willis, while the neurohypophysis and adenohypophysis receives blood from the lower and upper, respectively hypophyseal arteries. The capillary plexus drains the inferior hypophyseal artery dural sinus although some of these capillaries as neural stem vein "short" door that drain into the anterior pituitary gland. SHEEHAN'S SYNDROME During pregnancy, there is an increase of approximately 50% in volume of the pituitary gland. This is mainly due to hyperplasia of prolactin secreting Lactotrophs to prepare the breasts for lactation. Thus, while the volume of the pituitary fossa in
- 9. which enhances the pituitary gland fails to support this growth. The sudden drop in blood pressure after an event such as a postpartum hemorrhage causes ischemia of the gland, cell damage and edema. In turn, edema results in swelling of the pituitary gland (which is already enlarged at Lactotrophs hyperplasia) further restricting the normal flow of blood to the gland. The result is a gland that causes stroke in the loss of their secretions. GROWTH DEFICIENCY AND SOMATOTROPIN An example to facilitate understanding: age is plotted on the (X) axis horizontal. Two sets of normal data are plotted. Height (the upper set of curves) is shown on the left vertical (Y) and weight (lower set of curves) on the Y axis to the right. A boy, "this case was initially referred to as' failure to thrive", a term generally used for children under 2 years of age who are not focused on weight (e.g., leaning his height). To interpret this case, it is necessary to understand the use of growth charts; the initial presentation was closer to the third percentile for weight, than third percentile for height. In other words it is a child of short stature and weighing. Thus, he was unable to move, he was not getting growth. Wtith parents on the 25th percentile, it would have been expected, all other things being equal, also growing along that line. Postnatal growth never matches this with just a 20-fold increase in mass and an increase of 3-4 times in length. In childhood, there is a period of rapid growth followed by a period of steady growth, with a mid-childhood acceleration, the pubertal growth spurt and a deceleration phase until final height. In involutionary years, there is a period of shrinkage, which reflects the changes of bone marrow fat. Intrauterine growth is regulated by the endocrine system, maternal and genetic factors, although the determinants of pre-natal growth are poorly understood. GH concentrations in fetal plasma is very high and even children with GH deficiency hormone, and even those with anencephaly, may have normal body length at birth. Maternal (uterine) influences have been difficult to define, but poor maternal nutrition is the most important factor that leads to low birth weight and duration worldwide. Alcohol intake and smoking are other adverse factors on fetal growth and maternal infections such as rubella, toxoplasmosis and cytomegalovirus lead to many changes, and short stature. THE GH AND IGF: The IGF family consists of 3 members (insulin, IGF-1 and IGF-2) common share structural similarities. There are variant forms of the IGF. The IGF-1 and IGF-2 also
- 10. has metabolic functions, but also play a major role in fetal growth, maturation, infants, children and juveniles. Dr. João Santos Caio Jr. Endocrinologia – Neuroendocrinologista CRM 20611 Dra. Henriqueta V. Caio Endocrinologista – Medicina Interna CRM 28930 AUTORIZADO O USO DOS DIREITOS AUTORAIS COM CITAÇÃO DOS AUTORES PROSPECTIVOS ET REFERÊNCIA BIBLIOGRÁFICA. Como saber mais: 1. Os genes para essas proteínas provavelmente evoluíram de um ancestral comum, mesmo que os genes sejam localizados em cromossomos diferentes (cromossomo 6 para prolactina e cromossomo 17 para GH)... http://hormoniocrescimentoadultos.blogspot.com 2. Os genes para GH, prolactina e lactogênio placentário têm uma organização estrutural eliminada na excisão e é chamada de íntron (o processo de reconhecimento de introns e exons em genes para definir quais trechos serão transcritos em uma cadeia de RNA guarda uma admirável complexidade) separando cinco éxons... http://longevidadefutura.blogspot.com 3. É um segmento de DNA de um gene eucarioto cuja transcrição sobrevive ao processo de excisão (ou splicing)... http://imcobesidade.blogspot.com Referências Bibliográficas: Caio Jr, João Santos, Dr.; Endocrinologista, Neuroendocrinologista, Caio,H. V., Dra. Endocrinologista, Medicina Interna – Van Der Häägen Brazil, São Paulo, Brasil; Lee SL, Sadovsky Y, Swirnoff AH, Polish JA, Goda P, et al. 1996. Luteinizing hormone deficiency and female infertility in mice lacking; the transcription factor NGFI-A (Egr-1); Science 273:1219–21; Li S, Crenshaw EB III, Rawson EJ, Simmons; DM, Swanson LW, Rosenfeld MG. 1990; Dwarf locus mutants lacking three pituitary cell-types result from mutations in the POUdomain gene pit-1. Nature 347:528–33 Lin CR, Koussi C, O’Connell S, Briata P, Szeto D, et al. 1999; Pitx2 regulates lung asymmetry, cardiac positioning and pituitary and tooth morphogenesis. Nature 401:279–82 Lin SC, Li S, Drolet DW, Rosenfeld MG. 1994; Pituitary ontogeny of the Snell dwarf mouse reveals Pit-1-independent and Pit-1- dependent origins of the thyrotrope. Development 120:515–22; Lin SC, Lin CR, Gukovsky I, Lusis AJ, Sawchenko PE, Rosenfeld MG. 1993.
- 11. Molecular basis of the little mouse phenotype and implications for cell type-specific growth. Nature 364:208–13 Lipkin SM, Naar AM, Kalla KA, Sack RA, Rosenfeld MG. 1993. Identification of a novel zinc finger protein binding a conserved element critical for Pit-1-dependent growth hormone gene expression. Genes Dev. 7:1674–87; Logan M, Tabin CJ. 1999. Role of Pitx1 upstream of Tbx4 in specification of hindlimb identity. Science 283:1736–39 Lu MF, Pressman C, Dyer R, Johnson RL, Martin JF. 1999. Function of Rieger syndrome gene in left-right asymmetry and craniofacial development. Nature 401: 276–78; Martin GR. 1998. The roles of FGFs in the early development of vertebrate limbs. Genes Dev. 12:1571–86 Mead PE. Contato: Fones: 55 11 5087-4404 ou 96197-0305 Nextel: ID:111*101625 Rua Estela, 515 - Bloco D - 12º andar - Conj. 121/122 Paraiso - São Paulo - SP - Cep 04011-002 e-mails: drcaio@vanderhaagenbrasil.com drahenriqueta@vanderhaagenbrasil.com vanderhaagen@vanderhaagenbrasil.com Site Van Der Häägen Brazil www.vanderhaagenbrazil.com.br www.clinicavanderhaagen.com.br www.crescimentoinfoco.com www.obesidadeinfoco.com.br http://drcaiojr.site.med.br http://dracaio.site.med.br Joao Santos Caio Jr http://google.com/+JoaoSantosCaioJr google.com/+JoãoSantosCaioJrvdh Video http://youtu.be/woonaiFJQwY Google Maps: http://maps.google.com.br/maps/place?cid=5099901339000351730&q=Van+Der+Haagen+Brasil&hl= pt&sll=-23.578256,46.645653&sspn=0.005074,0.009645&ie =UTF8&ll=-23.575591,- 46.650481&spn=0,0&t = h&z=17
