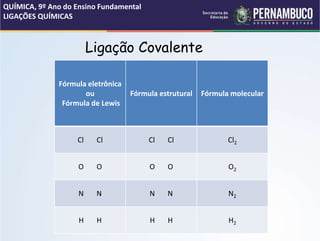
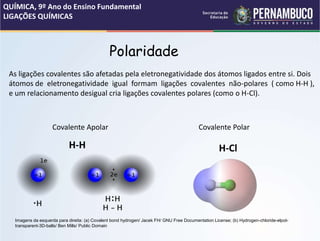
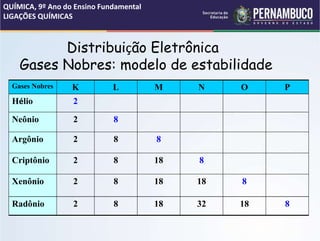
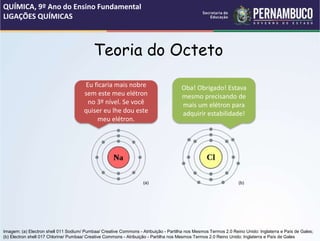
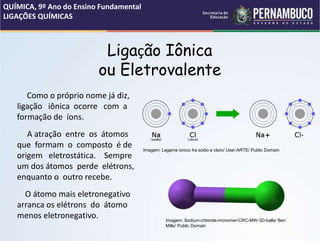
O documento discute os conceitos de estrutura atômica, ligações químicas e tipos de ligação. Apresenta os modelos atômicos de Thomson e Dalton, as partículas subatômicas como prótons, elétrons e núcleo. Aborda as ligações iônica, covalente e metálica, explicando suas características e formação de íons. Também discute a polaridade em ligações covalentes e fornece exemplos de substâncias com diferentes tipos de ligação.








![Fórmula de um
Composto Iônico
Para escrever a fórmula de um composto iônico, é preciso descobrir a
carga do íon formada pelos elementos presentes e levar em conta que a
carga total do composto é nula.
[ Cátion x+ ] y [Ânion y- ] x
O cátion é escrito à esquerda e o ânion, à direita.
[ Ca 2+ ]1 [ F - ]2 CaF2
QUÍMICA, 9º Ano do Ensino Fundamental
LIGAÇÕES QUÍMICAS](https://image.slidesharecdn.com/ligaesqumicas1-220816094214-6287812c/85/Ligacoes-quimicas-1-ppt-16-320.jpg)