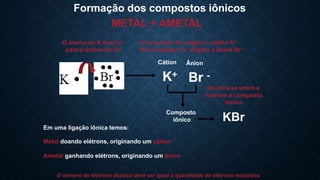
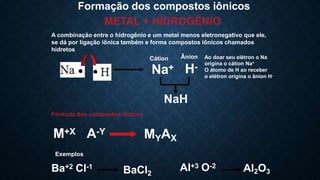
Este documento discute os diferentes tipos de ligação química: iônica, covalente e metálica. A ligação iônica envolve a transferência de elétrons entre átomos, formando íons e compostos iônicos. A ligação covalente envolve o compartilhamento de elétrons entre átomos, formando moléculas. A ligação metálica envolve a dispersão de elétrons entre átomos de metais, formando ligas metálicas.