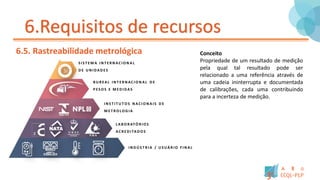
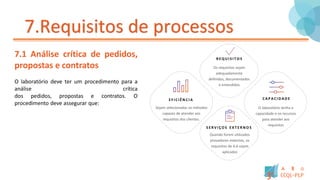
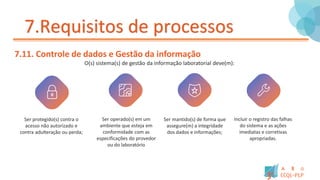
Este documento fornece um resumo dos principais pontos da norma ISO/IEC 17025:2018 para laboratórios de ensaio e calibração. Ele descreve os requisitos gerais para a estrutura, gestão, processos, recursos e competência que laboratórios devem ter para demonstrar que operam de forma competente e geram resultados válidos.