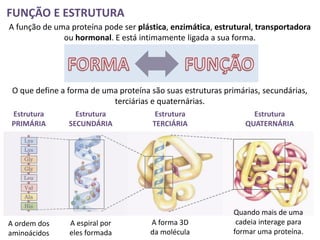
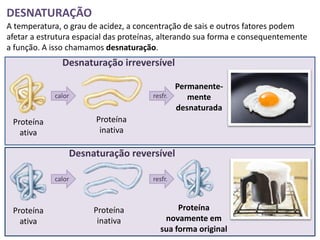
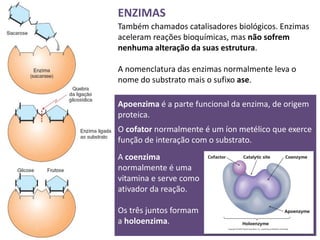
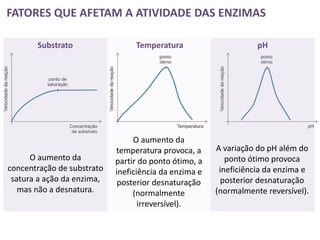
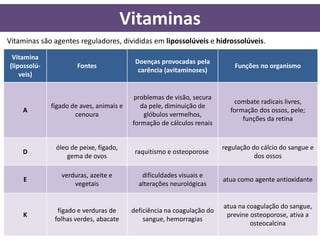
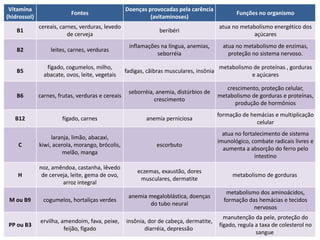
O documento discute as proteínas e vitaminas. As proteínas são formadas por cadeias de aminoácidos unidos por ligações peptídicas. As vitaminas são divididas em lipossolúveis e hidrossolúveis e desempenham funções importantes no organismo como o metabolismo energético e a formação de hemácias. As enzimas são proteínas que aceleram reações bioquímicas e podem ser afetadas por fatores como temperatura e pH.