O documento descreve:
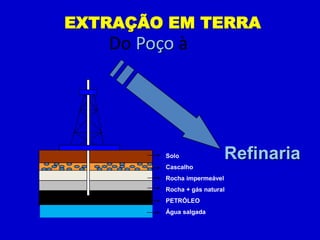
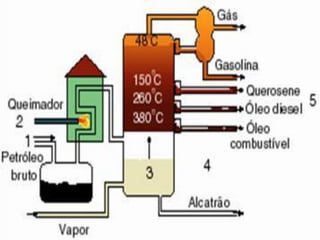
1) O processo de extração do petróleo, desde a prospecção até o refino e distribuição.
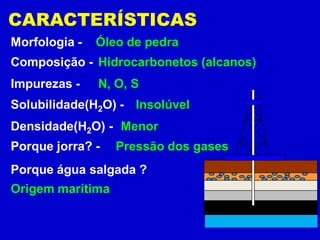
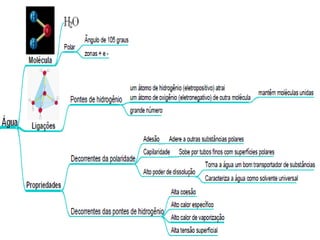
2) As características do petróleo como sua morfologia, composição, solubilidade e origem.
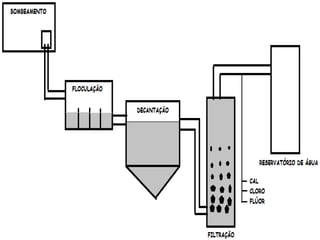
3) As etapas do refino como filtração, decantação e destilação fracionada para separar as frações do petróleo.