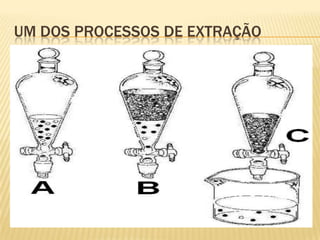
Este documento descreve o processo de extração com solventes, no qual substâncias são extraídas de um material usando sua solubilidade em diferentes solventes. Explica que a extração envolve colocar uma solução em contato com um solvente imiscível para transferir solutos de um solvente para outro. Também fornece exemplos como a extração de óleos de plantas e a preparação de café.