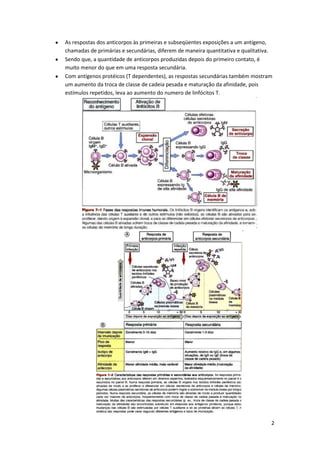
A imunidade humoral é mediada por anticorpos e é importante para neutralizar microorganismos extracelulares e toxinas. As células B produzem anticorpos específicos em resposta a antígenos e requerem a ajuda de células T para respostas eficazes contra antígenos proteicos. A ativação das células B envolve a ligação do antígeno ao receptor, sinalização intracelular e estímulos secundários de células T e complemento, levando à proliferação e diferenciação das células B.