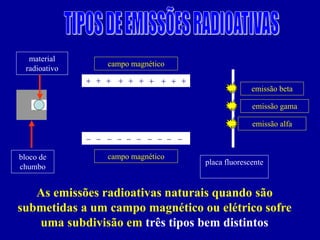
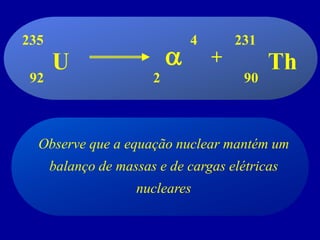
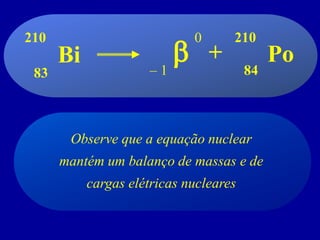
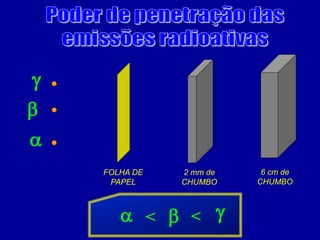
O documento discute o uso da radioatividade na medicina, agricultura, arqueologia, geologia e como fonte de energia. A radioatividade é usada no diagnóstico e tratamento de doenças, na datação de fósseis e rochas, e na geração de energia em reatores nucleares. Os principais tipos de radiação são alfa, beta e gama.