Este documento descreve vários tipos de reações químicas, incluindo:
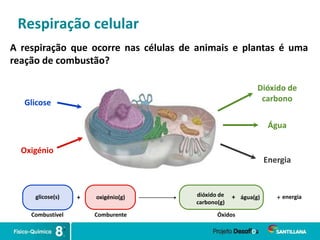
1) Reações de combustão ocorrem quando um combustível reage com um comburente como o oxigênio, liberando energia.
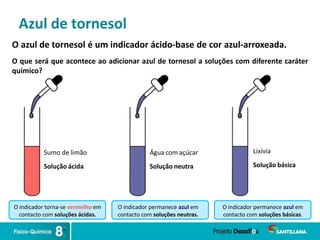
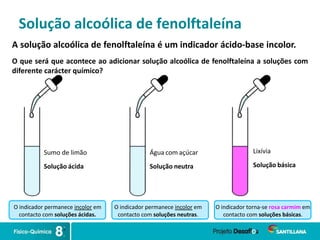
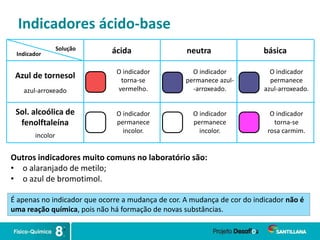
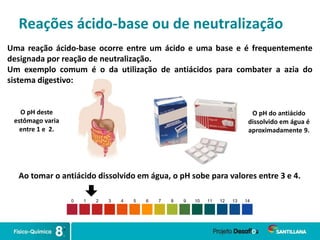
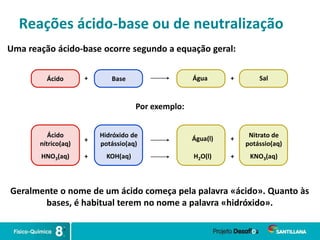
2) Reações ácido-base ocorrem quando ácidos e bases se neutralizam, formando água e sais.
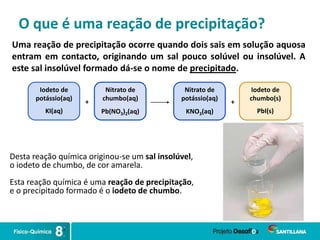
3) Reações de precipitação ocorrem quando sais insolúveis se formam ao se misturarem sais solúveis em solução.