1) O objetivo era determinar experimentalmente a concentração de ácido acético em vinagre usando titulação potenciométrica e condutométrica.
2) Foram realizadas titulações de uma amostra de ácido acético e de vinagre, obtendo curvas de pH, condutividade e suas derivadas em função do volume de NaOH adicionado.
3) A análise dos dados permitiu calcular a constante de acidez do ácido acético e a concentração no vinagre, encontrando valores próximos por ambos


![8 0,1023 0,12958 5,22 0,32 0,04
8,5 0,1085 0,139242 5,38 0,36 0,1
9 0,113 0,1469 5,56 0,46 0,98
9,5 0,1192 0,156947 5,79 1,44 3,46
10 0,1239 0,1652 6,51 4,9 0,6
10,1 0,1259 0,168286 7 5,5 9,8
10,2 0,1277 0,171118 7,55 15,3 -11,4
10,3 0,1166 0,156633 9,08 3,9 1,1
10,4 0,1273 0,171431 9,47 5 -3,2
10,5 0,1301 0,175635 9,97 1,8 -0,8
10,6 0,1339 0,181211 10,15 1 0,8
10,7 0,13 0,176367 10,25 1,8 -1
10,8 0,1411 0,191896 10,43 0,8 0,1
10,9 0,1421 0,19373 10,51 0,9 -0,3
11 0,1442 0,197073 10,6 0,6 -0,28
11,5 0,1576 0,218013 10,9 0,32 -0,06
12 0,1619 0,22666 11,06 0,26 -0,08
12,5 0,18 0,255 11,19 0,18 -0,04
13 0,202 0,289533 11,28 0,14 0
13,5 0,221 0,32045 11,35 0,14 -0,06
14 0,237 0,3476 11,42 0,08 0,06
14,5 0,242 0,358967 11,46 0,14
15 0,26 0,39 11,53
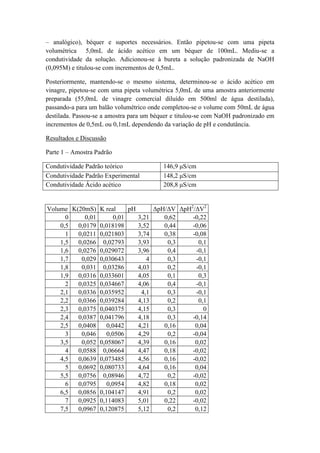
A partir dos dados, obteve-se os gráficos de condutância versus volume, pH versus
volume, 1˚ derivada e 2˚ derivada, que podem ser observados nos anexos: 1,2,3 e 4.
Cálculo a partir da Concentração de ácido acético pela Condutância:
Veq. = 10,4
[NaOH] = 0,095M
CNaOHx VNaOH = CHAc x VHAc
0,095mol/L x 10,4 mL = CHAc x 55mL
CHAc= 1,79.10-2
mol/L
Como a amostra foi diluída:
1,79.10-2
mol/L x 55mL= C2HAc x 5mL
C2HAc= 0,1969mol/L
Cálculo do pKa pela condutividade obtida experimentalmente:
Sendo
α=Λm/Λ∞](https://image.slidesharecdn.com/potenciometriarelat-130723073034-phpapp01/85/Potenciometria-relat-4-320.jpg)