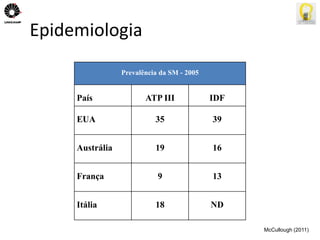
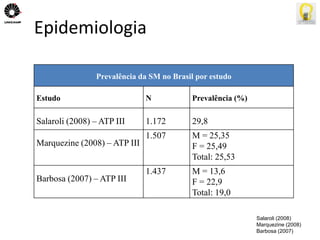
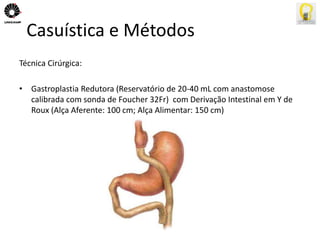
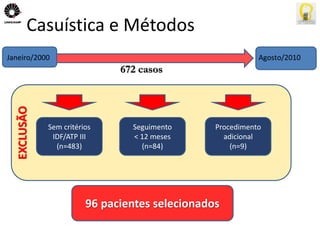
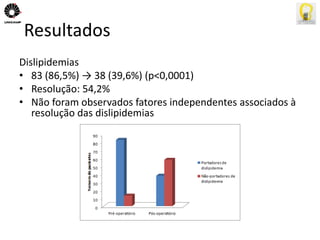
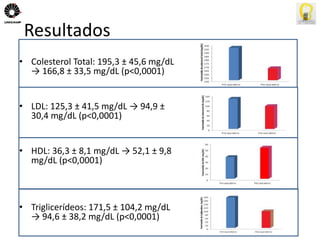
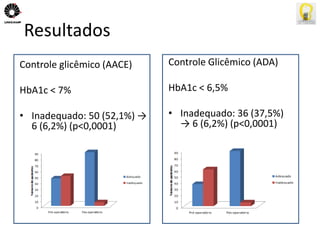
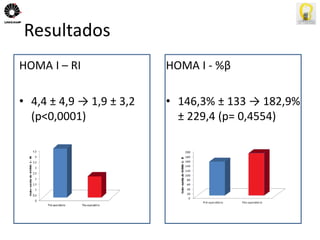
O documento descreve uma tese de mestrado sobre o impacto do bypass gástrico em Y de Roux na síndrome metabólica. O resumo apresenta os objetivos gerais de caracterizar os pacientes operados e descrever o impacto da cirurgia na síndrome metabólica e suas comorbidades clínicas e bioquímicas.