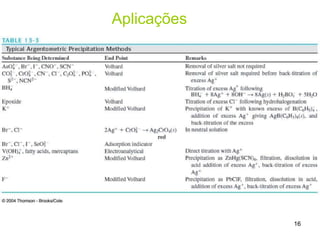
Este documento descreve diferentes métodos para titulações argentimétricas utilizando indicadores químicos, incluindo: 1) Método de Mohr que usa cromato como indicador, formando um precipitado vermelho de Ag2CrO4; 2) Método de Fajans que usa indicadores de adsorção como a fluoresceína; 3) Método de Volhard que usa íons Fe3+ e tiocianato para titular Ag+ de forma colorida.

![Método de Mohr
K ps [Ag ][Cl ]
]
2
2
K [Ag ] [CrO
ps 4
[Ag
] 1,35x105
mol L1
2
Kps
O cromato serve como indicador para determinações de cloreto,
brometo e cianeto por meio da reação com íons prata formando um
precipitado vermelho indicativo do ponto final.
Ag+
(aq) + C𝑙
-
(aq) ⇌ AgC𝑙
(s) (branco)
2Ag+
(aq) + CrO4
2- ⇌Ag CrO (vermelho)
(aq) 2 4(s)
A concentração de Ag+ no ponto de equivalência numa titulação de
cloreto comAgNO3 é:](https://image.slidesharecdn.com/aula-6-titulao-de-precipitao-230131220415-97e90947/85/aula-6-titulacao-de-precipitacao-pptx-2-320.jpg)
![A concentração de CrO4
2- necessária para a formação de Ag2CrO4 é:
Uma quantidade de CrO4 deveria ser adicionada momentos antes do
2-
P.E. do AgC𝑙
.
No entanto, a solução de cromato produz uma cor amarela intensa,
que mascara a formação do precipitado vermelho.
Assim sendo, concentrações menores de cromato são adicionadas e
um excesso de AgNO3 é necessário antes que a precipitação de
Ag2CrO4 ocorra.
6,6x103
mol L1
2 1,2x1012
]
[Ag
]2
(1,35x105
)2
[CrO4
Kps
Significante para concentrações < 0,1 mol L-1
3
ERRO SISTEMÁTICO POSITIVO](https://image.slidesharecdn.com/aula-6-titulao-de-precipitao-230131220415-97e90947/85/aula-6-titulacao-de-precipitacao-pptx-3-320.jpg)

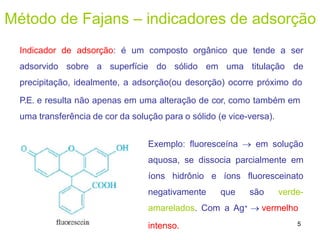

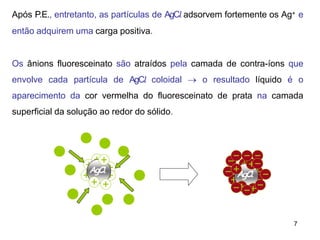





![Método de Volhard – íons Fe(III)
Utiliza SCN- para titular Ag+ na presença de ions Fe3+ como indicador.
Ag+
(aq) + C𝑙
-
(aq) ⇌ AgC𝑙
(s)
Ag+
(aq) + SCN-
(aq) ⇌ AgSCN(s)
A titulação deve ser realizada em solução ácida para prevenir a
precipitação com íons Fe3+ como hidróxido.
Fe3+ + SCN- ⇌ FeSCN2+
(aq) (aq)
vermelho
[FeSCN 2
]
13
3
[Fe3
][SCN
]
K f 1,05x10 ](https://image.slidesharecdn.com/aula-6-titulao-de-precipitao-230131220415-97e90947/85/aula-6-titulacao-de-precipitacao-pptx-13-320.jpg)