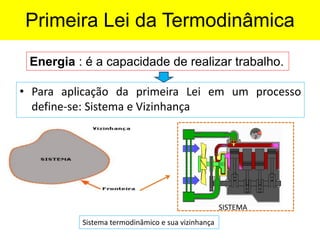
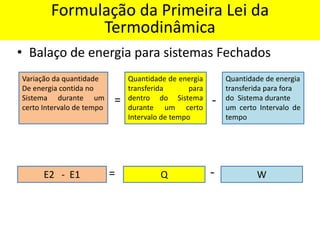
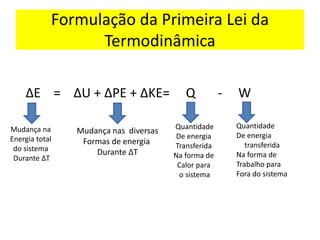
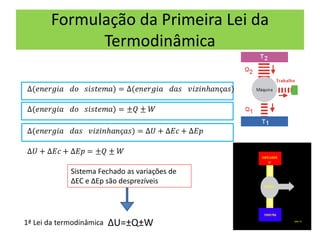
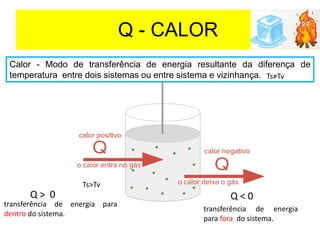
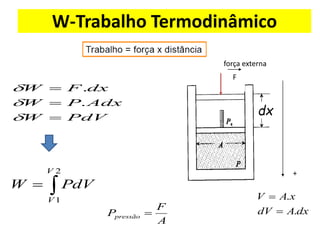
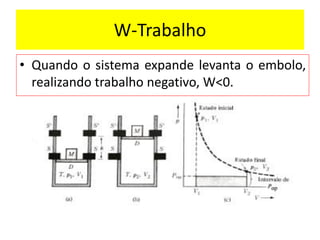
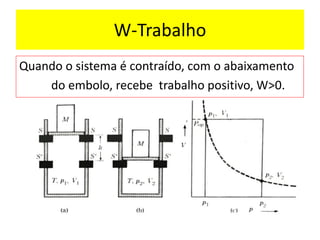
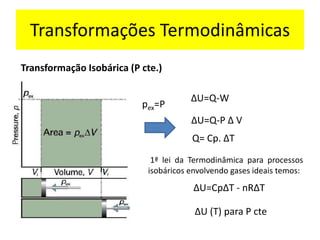
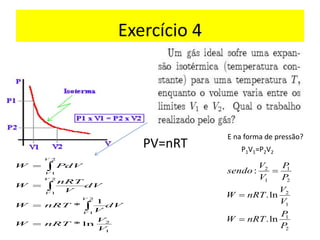
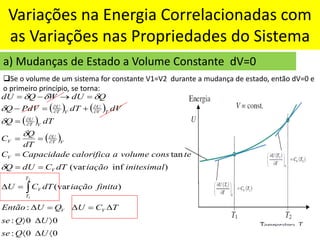
O documento aborda a primeira lei da termodinâmica, enfatizando os conceitos de sistema, vizinhança, calor, trabalho e energia interna. Ele apresenta a formulação da lei com equações relevantes e exemplos práticos para ilustrar transformações termodinâmicas. O objetivo final é que os alunos compreendam os princípios da conservação de energia e a aplicação destes em exercícios.