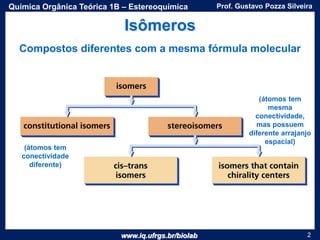
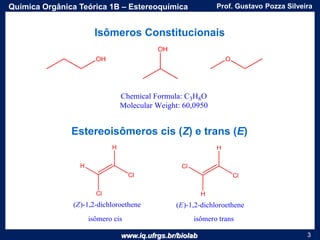
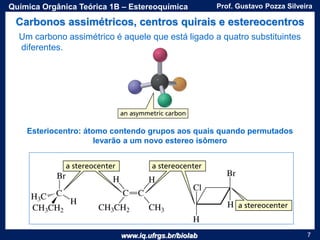
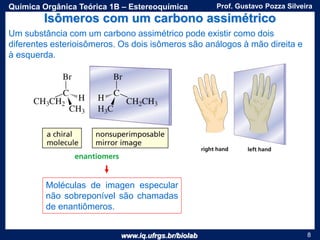
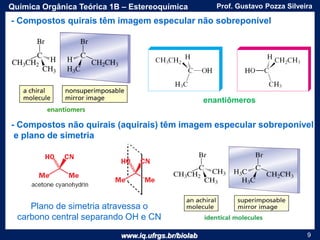
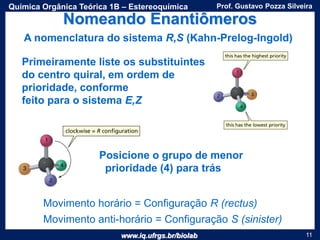
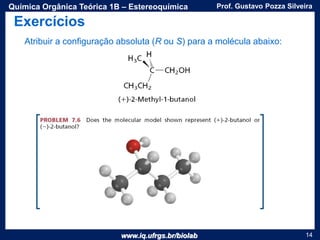
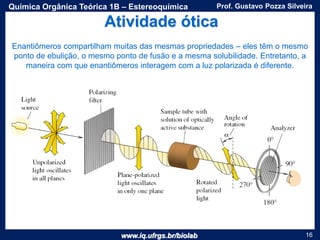
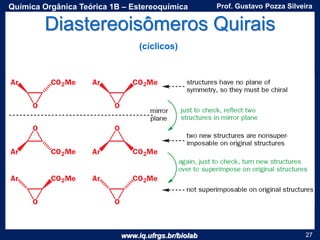
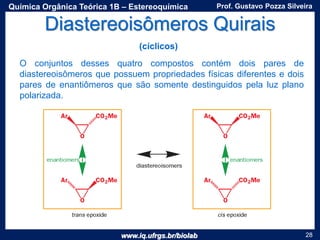
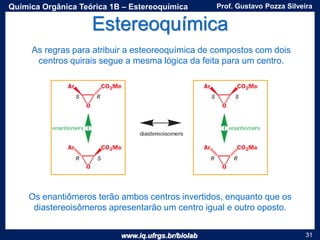
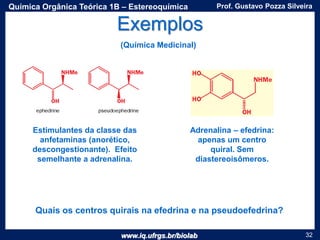
O documento apresenta uma aula sobre estereoquímica ministrada pelo professor Gustavo Pozza Silveira. Aborda conceitos como isomeria, quiralidade, centros estereogênicos, enantiômeros, diastereômeros, atividade óptica e métodos de representação tridimensional de moléculas. Inclui também exemplos e exercícios sobre a aplicação destes conceitos.