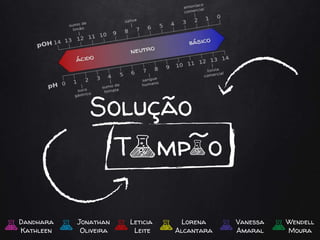
Solução tampão
- 2. Uma solução tampão ou solução Tamponada é aquela que resiste bem a variações de pH quando nela introduzimos uma pequena quantidade de ácido ou base. São muito importantes em sistemas químicos e biológicos!
- 3. Os sistemas biológicos (células individuais, fluidos orgânicos e sistemas de órgãos) regulam o seu funcionamento, relativamente ao pH, num processo denominado homeostase ácido-base. O pH do sangue (±7,4) é o pH fisiológico. Exemplo da importância da manutenção do pH: Enzimas e outras proteínas podem ser inactivadas ou mesmo destruídas se colocadas num meio com pH ≠ pH óptimo.
- 4. H2O H2O SOLUÇÃO FINAL SOLUÇÃO FINAL PH=7 PH=7 1l 1l Adicionado 0,01 mol de HCL Adicionado 0,01 mol de NaOH Sistema comum PH=2 PH=12 O Ph baixou 5 unidades O Ph aumentou 5 unidades
- 5. 0,1 mol CH3 COOH + 0,1 mol CH3COONa SOLUÇÃO FINAL SOLUÇÃO FINAL PH=4,74 PH=4,74 1l 1l Adicionado 0,01 mol de HCL Adicionado 0,01 mol de NaOH Sistema tamponado PH=4,65 PH=4,83 O Ph baixou 0,09 unidades O Ph aumentou 0,09 unidades 0,1 mol CH3 COOH + 0,1 mol CH3COONa
- 6. A solução tampão dá conta de gastar todo o H+ ou OH- adicionado, impedindo bruscas variações de pH. HCL 0,1 molL-1 HCL 0,1 molL-1 NH4CL NH4 + CL- NH3 + H2O NH4 + OH- Obs: A adição de H+ aumenta a [NH4+] A adição de OH- aumenta a [NH3 +] A base adicionada reage com o CH3COOH formando o CH3COO- CH3COOH CH3COO- A acido adicionado reage com o CH3COO- formando o CH3COOH
- 7. Podem ser preparadas dissolvendo-se em água: Um ácido fraco e um sal derivado dele. Ex.: CH3COOH/CH3COONa Uma base fraca e um sal dela derivado. Ex.: NH4OH/NH4Cl ou seja, NH3/NH4Cl
- 8. O ácido FRACO e seu ÂNION Exs.: CH3COOH/CH3COO-; H2CO3/HCO3-; HCN/CN- A base FRACA e seu CÁTION Ex.: NH4OH/NH4 + ou seja, NH3/NH4 +
- 9. Certos ânions não conseguem remover os íons H+, formando moléculas de ácido. É o que acontece, por exemplo, com o ânion Cl-: como o ácido clorídrico que seria formado é forte, ele não possui a tendência de se apresentar, em solução aquosa, na forma de moléculas de HCl. Portanto, uma solução contendo um ácido forte e um sal derivado desse ácido não atua como um tampão. Uma solução contendo uma base forte e um sal derivado dessa base não atua como um tampão, pois seu cátion não consegue remover os íons OH-.
- 10. Tampão ácido fraco/ânion do ácido Tampão base fraca/cátion da base poH = pKb + log [sal] [base] EQUAÇÃO DE HENDERSON HASSELBALCH ►pK se refere ao logaritmo negativo de uma constante de equilíbrio . Quando K aumenta, sua função p decresce e vice-versa. ► quanto maior o Ka e menor o pKa mais forte é o ácido.
- 11. O sangue é uma mistura aquosa complexa com um pH tamponado a aproximadamente 7,4. Muitas das reações que ocorrem nos seres vivos são extremamentes sensiveis ao pH e só realizam-se em uma faixa estreita de pH.
- 13. Sangue humano: ligeiramente básico com umpH normal de 7,35 a 7,45 Desvio de faixa de pH: efeitos que rompem significativamente a estabilidade das menbranas das células, estruturas das proteínas e das atividades das enzimas Se o pH cai abaixo de 6,8 ou subir acima de 7,8 pode resultar em morte ACIDOSE : o pH cai abaixo de 7,35 ALCALOSE: o pH sobe acima de 7,45
- 14. H2PO4 -/HPO4 -2 e algumas ENZIMAS Exemplo de Outros tampões no sangue Sistema tampão usado para controlar o pH do sangue Sistema tampão ácido Carbonico – bicarbonato H2CO3 / HCO3- : são um par ácido base conjugado
- 15. Como Funciona ? Ácido carbônico / bicarbonato – 64% Proteína ácida / proteína básica – 7% Hemoglobina / oxihemoglobina -28% Fosfato monoácido / fosfato diácido – 1% O mais importante dos sistemas é o acido carbônico / bicarbonato, pois ativa diretamente na regulação do pH. Quando um acido é adicionado ao sangue o bicarbonato do tampão prontamente reage a ele; a reação produz um sal, formado com o sodio do bicarbonato e o acido carbônico. Essa reação diminui a quantidade de base e altera a relação entre o bicarbonato e o acido carbônico. O acido carbônico produzido pela reação do bicarbonato do tampão se dissocia em co2 e água, o co2 é eliminado nos pulmões recompondo a relação do sistema
- 16. Quando uma base invade o organismo, o ácido carbônico prontamente reage a ela, produzindo bicarbonato e água. O ácido carbônico diminui. Os rins aumentam a eliminação de bicarbonato ao invés do íon hidrogênio, reduzindo a quantidade de bicarbonato no organismo, para preservar a relação do sistema tampão. Ácidos e bases conjugadas: um ácido conjugado é a parte ácida de um par de espécies químicas (íons ou moléculas) que se formam em consequência da ionização de um ácido (HX) que perde um hidrogênio (H+). A parte básica que se forma após a transferência (X−) é chamada base conjugada. Os ácidos são doadores de prótons, e as bases são receptoras de prótons. A base conjugada ou o ácido conjugado é o que resulta depois que um ácido perde um próton ou que uma base ganha um próton, respectivamente.
- 17. ADIÇÃO DE ÁCIDO: A adição de H+ no sangue, faz com que esses íons de combinem com o HCO3 - proveniente do ácido e, principalmente do sal, originando o H2CO3. ADIÇÃO DE BASE: Se certa quantidade de íons OH- for introduzida no sangue, estes íons reagirão com o H+, retirando-o da solução, logo fará que o H2CO3 se ionize um pouco mais, produzindo H+ suficiente para neutralizar o OH- introduzido. Em nenhum dos casos, ocorre variações significativas de pH. O sangue transportado pelo sistema circulatório é mantido com pH de 7,4 pela ação de soluções-tampão
- 18. Base conjugada mais forte dentre as da tabelas Ácidosmaisforte dentreosda tabelas Base conjugada
- 19. Características de um tampão
- 20. É a quantidade de ácido ou base que um tampão pode neutralizar antes que o pH comece a variar de nível Depende da quantidade de ácido e base da qual o tampão é feito
- 22. Referências Bibliográficas Skoog. West. Holler. Crouch- Fundamentos de química analítica-tradução 8º Ed. Norte-amaricana. Ed. Thomson. FELTRE, Ricardo, 1928-. Química / Ricardo Feltre. — 6. Ed. — São Paulo: Moderna, 2004. P. W. Atkins e L. Jones, Princípios de Química: questionando a vida moderna e o meio ambiente, Bookman, Porto Alegre (2001). Ver Cap. 11. Biblioteca Digital de Ciências, 06/12/2015 <http://www.bdc.ib.unicamp.br/bdc/visualizarMaterial.php?idMaterial=464#.Vm R0DTA4RYw>
- 23. Centro Universitário Christus Seminário de Química 08 de Dezembro de 2015
