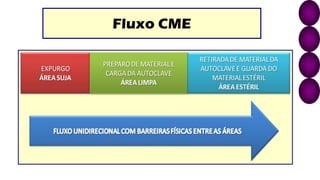
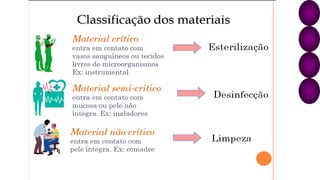
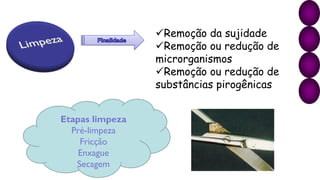
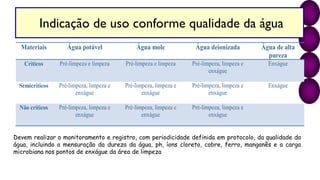
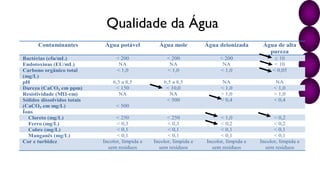
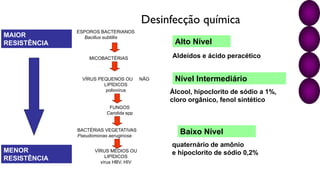
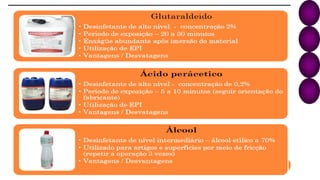
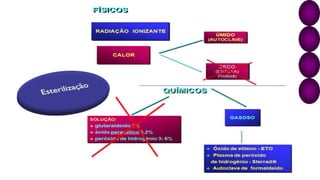
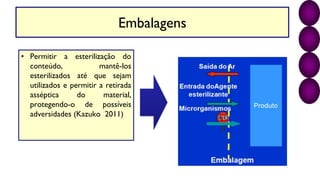
O documento discute os processos e procedimentos da Central de Material e Esterilização (CME), incluindo limpeza, desinfecção, esterilização e armazenamento de produtos para saúde. A CME deve garantir que os materiais sejam reprocessados de forma segura para proteger os pacientes e profissionais de saúde.