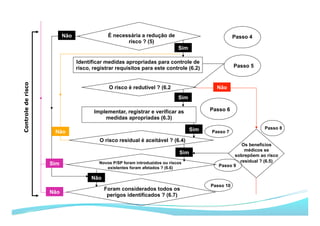
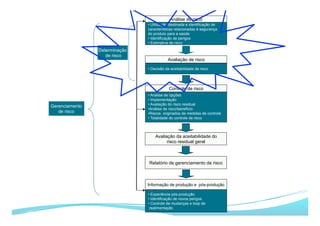
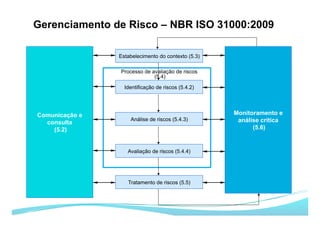
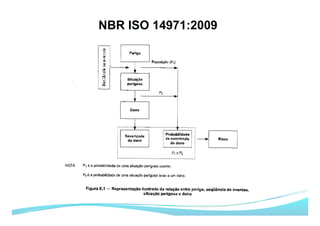
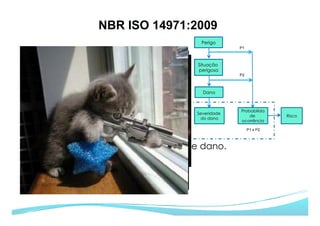
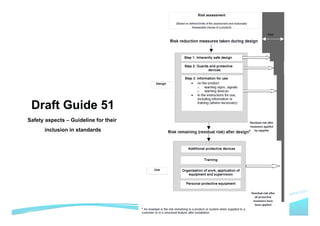
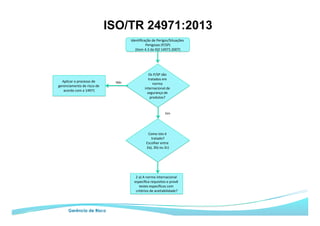
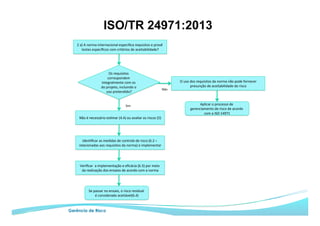
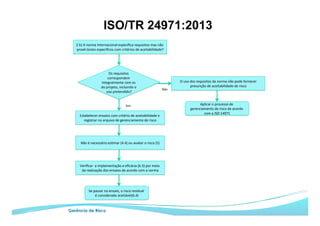
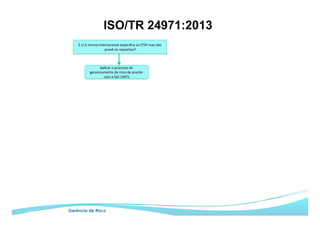
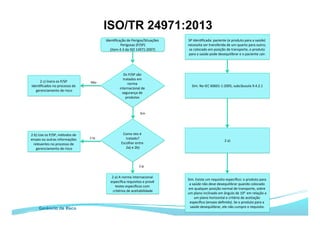
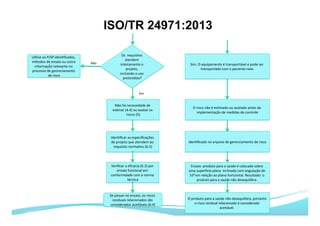
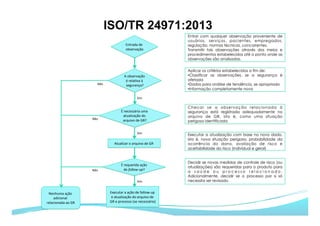
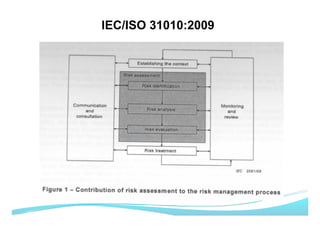
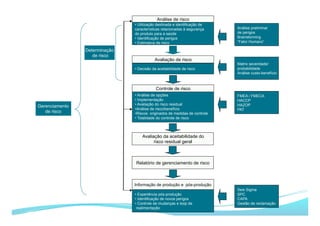
O documento apresenta as principais ferramentas para gerenciamento de risco, incluindo análise preliminar de perigos, FMEA/FMECA, HAZOP e Seis Sigma. Também discute os passos do processo de gerenciamento de risco segundo a NBR ISO 14971, como identificação de perigos, estimativa de risco, análise de risco e avaliação do risco residual.