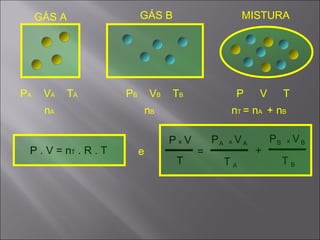
1) O documento descreve as leis dos gases ideais e suas transformações isotérmicas, isobáricas e isotérmicas.
2) A lei de Boyle afirma que sob pressão constante, o volume de um gás é diretamente proporcional à sua temperatura.
3) A lei de Charles afirma que sob volume constante, a pressão de um gás é diretamente proporcional à sua temperatura.