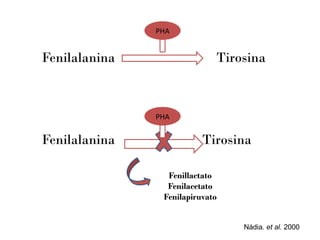
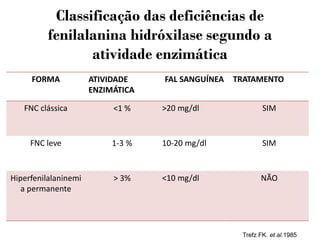
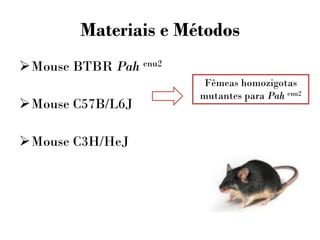
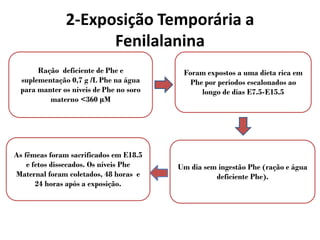
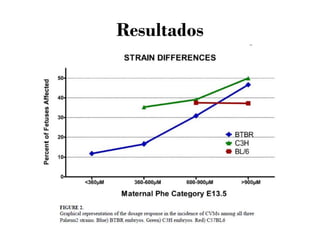
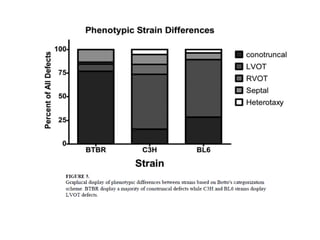
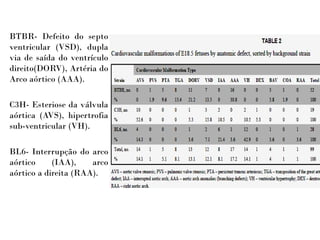
Este documento discute a teratogenicidade cardíaca em ratos com fenilcetonúria materna. Ele apresenta estudos que examinaram os efeitos de diferentes níveis de fenilalanina no sangue materno e períodos de exposição na ocorrência e tipo de malformações cardíacas nos fetos. Os resultados mostraram que a incidência e o tipo de defeito dependem da dose de fenilalanina e da linhagem genética dos ratos.