1) O documento discute a teoria dos gases, incluindo suas propriedades como volume, pressão e temperatura.
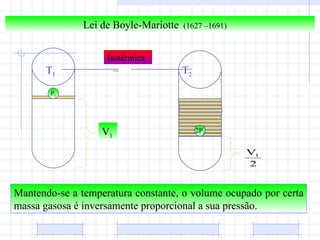
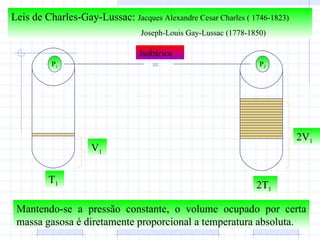
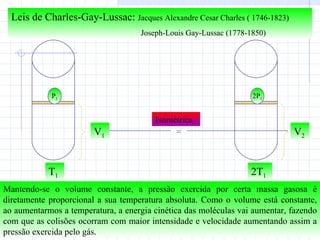
2) Ele explica as transformações de estado dos gases de acordo com as leis de Boyle, Charles e Gay-Lussac.
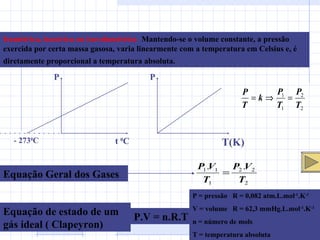
3) A hipótese de Avogadro e a equação dos gases ideais também são abordadas.