1) O documento discute a classificação de agentes biológicos pelo Ministério da Saúde brasileiro de acordo com o nível de risco à saúde;
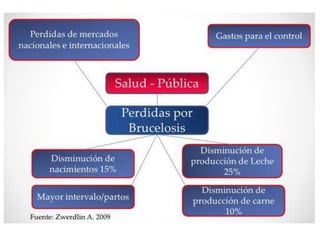
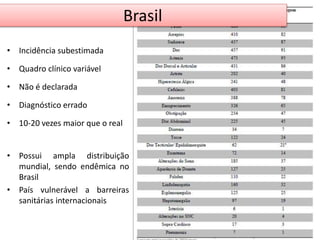
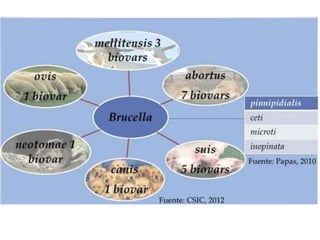
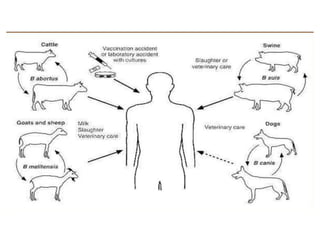
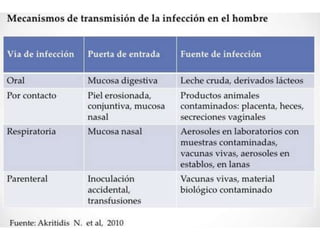
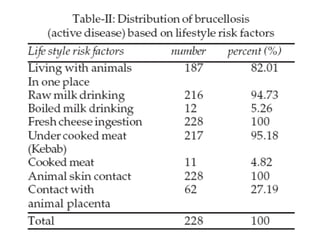
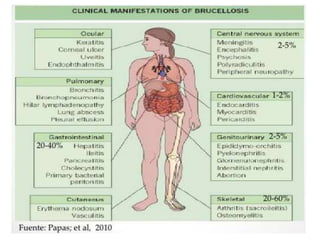
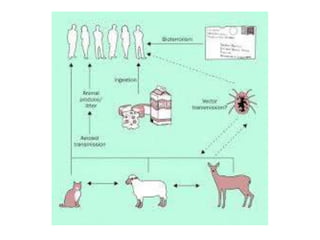
2) A brucelose é uma zoonose bacteriana causada por bactérias do gênero Brucella que pode infectar bovinos, suínos e humanos através do consumo de produtos de origem animal contaminados;
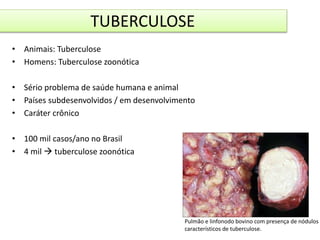
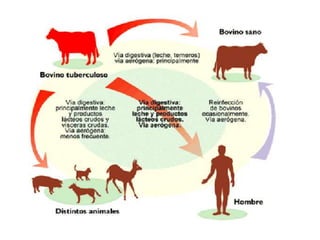
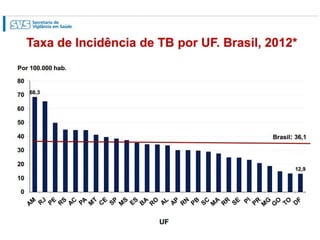
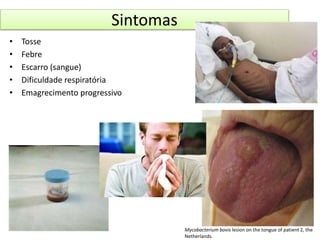
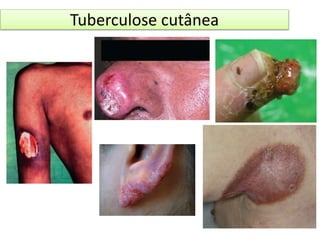
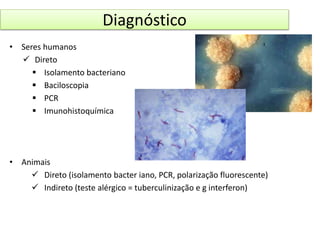
3) A tuberculose é uma zoonose causada pela bactéria Mycobacterium bovis que pode ser transmitida de bovinos para humanos