O documento descreve um novo método de eletrólise para produzir biodiesel a partir de óleos vegetais e óleos de cozinha usados a temperatura ambiente. O processo mostrou altos rendimentos de éster metílico de ácido graxo (>97%) mesmo na presença de até 2% de água. Os parâmetros como razão molar metanol/óleo, concentração de NaCl, tempo de eletrólise influenciaram o rendimento.


![Continuação
• Neste estudo, um método de eletrólise para a produção de BDF a partir de óleo
de milho e óleo de cozinha, contendo alto teor de água e a temperatura
ambiente na presença de NaCl é introduzida. Os efeitos da tensão de eletrólise,
proporções molar metanol / óleo, adição de cosolventes, concentração NaCl
contendo água , para a produção de FAME foram investigados.
• 2. Experimental
2.1. Produtos químicos
Óleo de milho de alta pureza, o metanol desidratado, tetrahidrofurano (THF) e
cloreto de sódio desidratados.
• Os valores do óleo foram determinados através de titulação padrão métodos
[19]. O peso molecular do determinada a partir
os valores de saponificação e ácido. Teor de água no óleo foi determinada com
titulador automático Karl-Fisher (MKC-610, Kyoto ). As propriedades físicas dos
óleos foram apresentados na Tabela 1
Tabela 1
Propriedades físicas de óleos usados.
Teor de de água (% peso) Acidez (mg KOH/g) Índice de saponificação (mgKOHg-1) Peso mol (g mol-1)
Óleo de milho <0,05 0,45 194,3 869,5
Oleo residual
• de cozinha 0,65 7,7 223,6 779,5](https://image.slidesharecdn.com/trabalhosntesedebiodieselutilizandoummtododeeletrlise-120315194658-phpapp01/75/Trabalho-sintese-de-biodiesel-utilizando-um-metodo-de-eletrolise-3-2048.jpg)


![continuação
• 3. Resultados e discursão.
• 3.1. Eletrólise
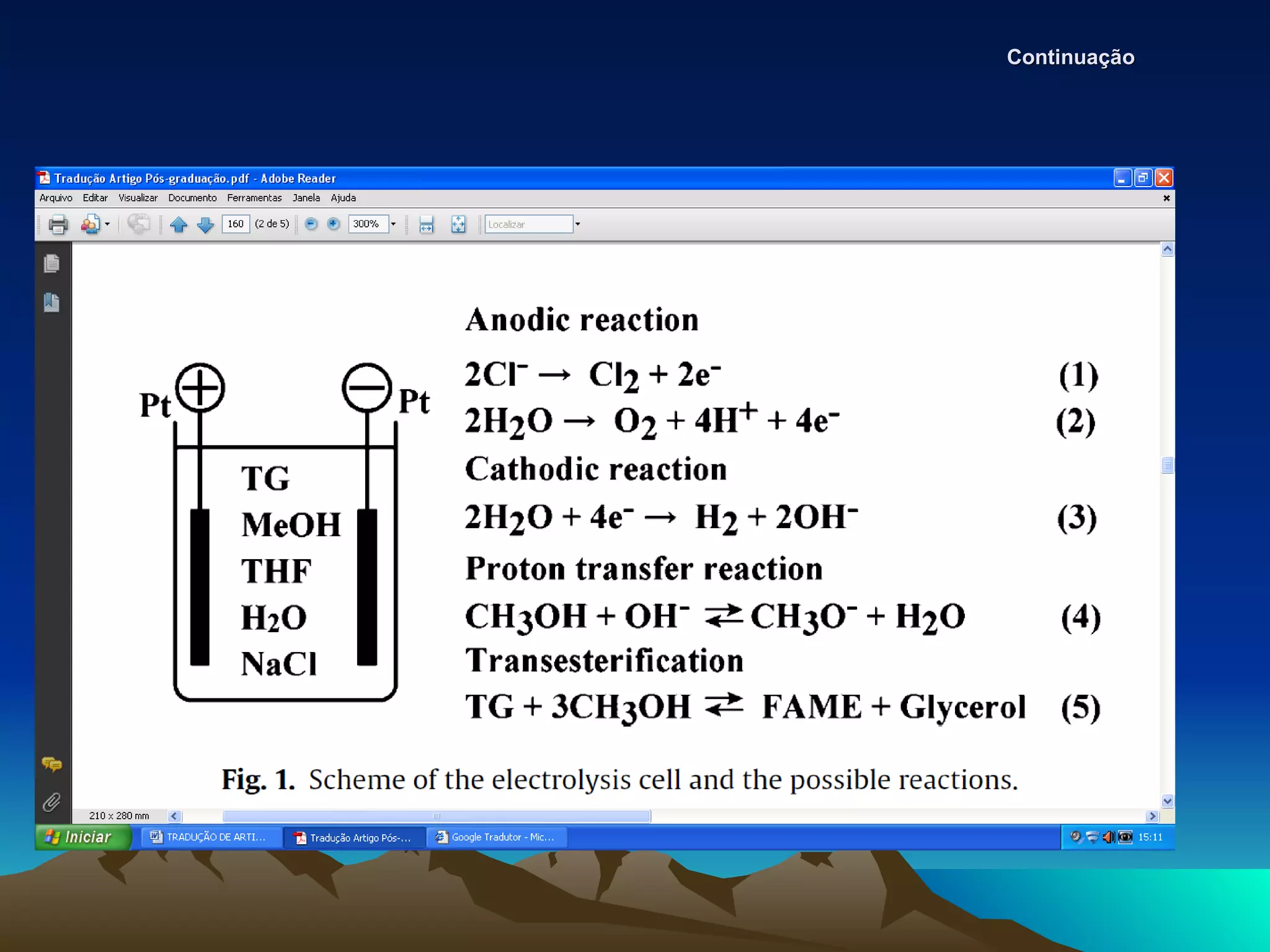
Como mostrado na figura. 1, quando a mistura de reação contendo NaCl e
H2O foi introduzido na célula de eletrólise, as evoluções da cloro ou oxigênio
pode ocorrer no ânodo (eqs. (1) e (2)). Em Por outro lado, os íons de
hidrogênio e hidroxila (Eq. (2)) foram formados no cátodo. A transesterificação
de triglicerídeos (TG), com metanol (Eq. (4)) requer uma espécie ativa, ou seja,
metóxido ion (CH3O), a fim de obter rendimento FAME razoável. Metóxido ion
podem se formar quando o metanol reage com um íon hidroxila (OH-) (Eq. (3)),
e uma vez formado, o íon metóxido é fortemente nucleofílico e os ataques a
metade carbonila nas moléculas glyceride para produzir ésteres metílicos [1,2].
Como resultado, BDF pode ser produzido usando este método de eletrólise.
3.2. Efeito da razão molar ( metanol / óleo )
• Os efeitos da composição da solução e da tensão de eletrólise
no rendimento FAME, primeirofoi investigado para a transesterificação
de óleo de milho. Fig. 2 (a), mostra os efeitos da relação molar do metanol / óleo
e a concentração de NaCl sobre a produção de FAME. Quando conc. de NaCl
menor 0,14 wt.% na presença de 2% (p/p) H2O, o rendimento aumentou FAME
um pouco com o aumento da relação molar metanol / óleo. O rendimento FAME
foi apenas 18,7% com um de relação molar =24 metanol / óleo. No entanto,
quando a concentração de NaCl foi aumentada para 0,28 wt.%, o rendimento
aumentou acentuadamente FAME com o aumento da relação metanol / óleo
molar. Transesterificação de triglicerídeos com metanol é uma reação de
equilíbrio [1].](https://image.slidesharecdn.com/trabalhosntesedebiodieselutilizandoummtododeeletrlise-120315194658-phpapp01/75/Trabalho-sintese-de-biodiesel-utilizando-um-metodo-de-eletrolise-7-2048.jpg)
