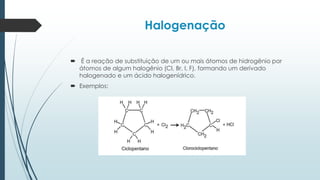
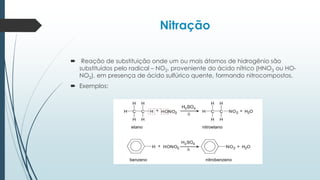
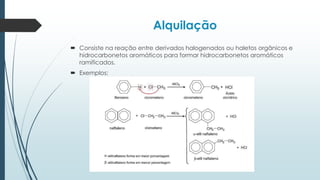
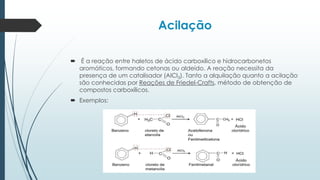
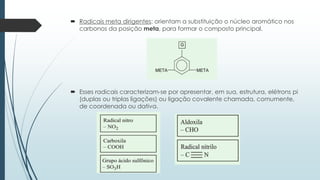
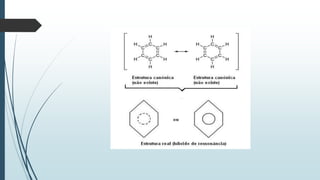
O documento discute reações orgânicas de substituição como halogenação, nitração, sulfonação, alquilação e acilação. Ele explica os mecanismos dessas reações, incluindo substituição por radicais livres e eletrófila. Também aborda efeitos como direcionamento e ressonância em compostos aromáticos.