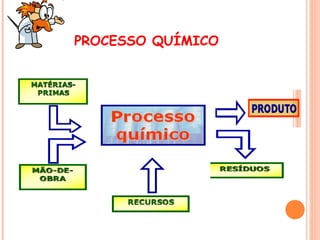
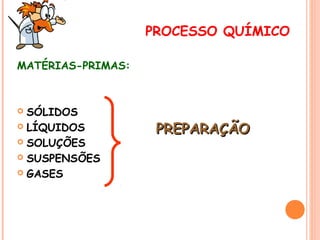
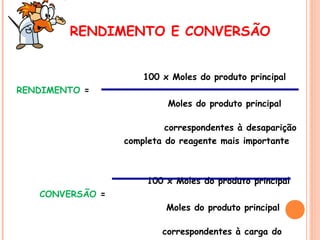
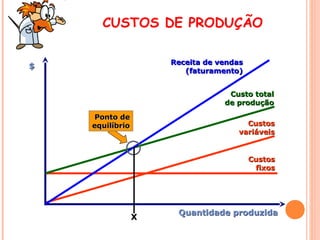
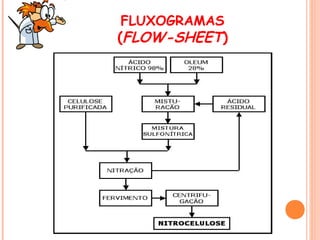
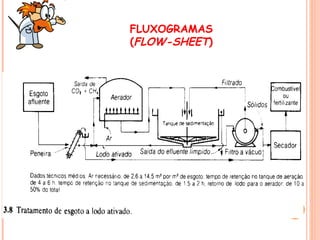
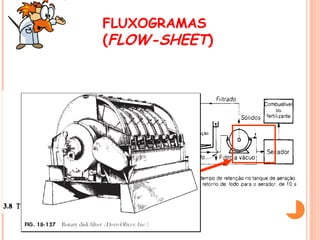
O documento apresenta um resumo sobre processos químicos inorgânicos industriais, incluindo: 1) Introdução aos processos contínuos e descontínuos e fluxogramas para representação dos processos; 2) Exemplos de indústrias como nitrogênio, fertilizantes, cloro e vidro; 3) Abordagem sobre reações químicas, rendimentos, conversões e custos de produção.