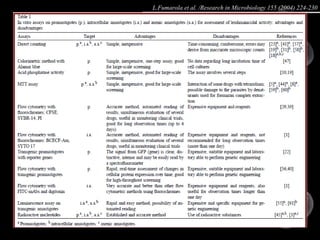
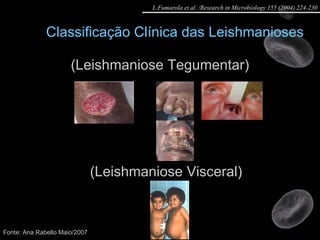
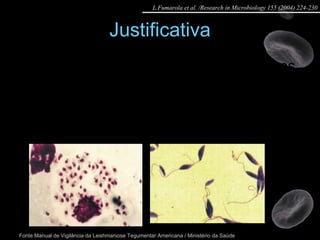
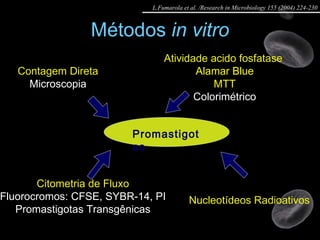
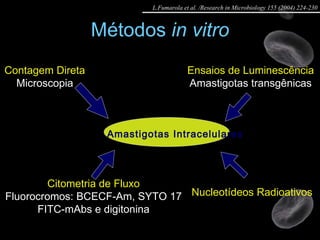
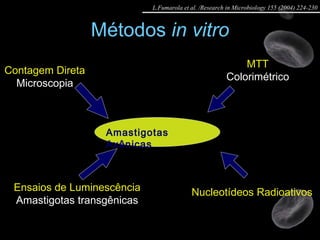
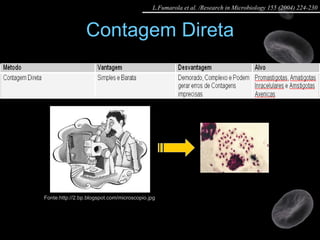
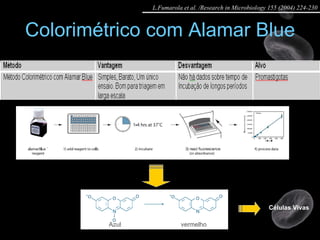
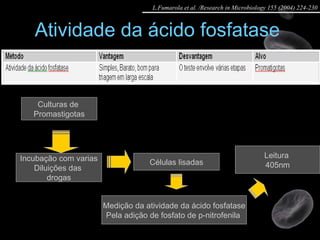
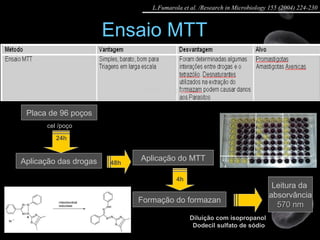
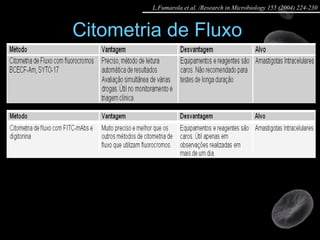
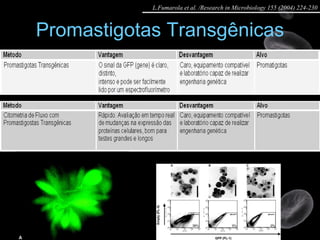
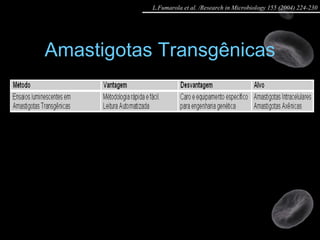
Artigo 01: Ensaios in vitro realizados em Leishmania spp para avaliar a atividade de drogas contra promastigotas e amastigotas utilizando diversos métodos como contagem direta, colorimétricos e citometria de fluxo.
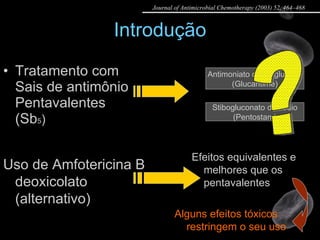
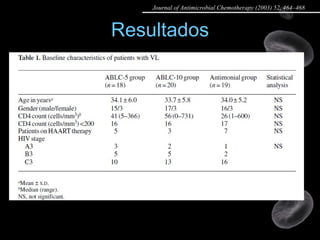
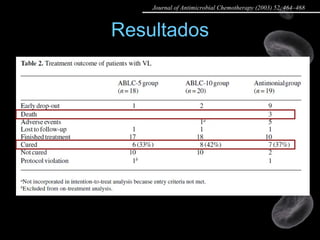
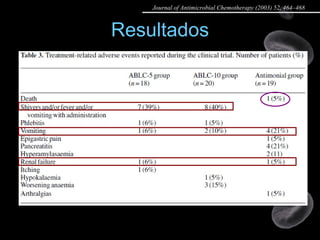
Artigo 02: Ensaio clínico multicêntrico e randomizado comparando a eficácia e tolerabilidade de duas doses de anfotericina B lipossomal com antimoniato de meglumina no tratamento da leishmaniose visceral em pacientes portadores de HIV.











![Nucleotídeos Radioativos [3H]-timidina é incorporada ao DNA durante a divisão celular. L.Fumarola et al. /Research in Microbiology 155 (2004) 224-230](https://image.slidesharecdn.com/cristianoseminriotoxicolo-13208908937729-phpapp02-111109201046-phpapp02/85/Cristiano-SeminaRio-Toxicolo-30-320.jpg)