Segunda Lei Da TermodinâMica
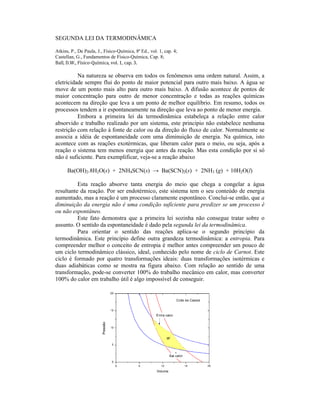
- 1. SEGUNDA LEI DA TERMODINÂMICA Atkins, P., De Paula, J., Físico-Química, 8ª Ed., vol. 1, cap. 4; Castellan, G., Fundamentos de Físico-Química, Cap. 8; Ball, D.W., Físico-Química, vol. 1, cap. 3. Na natureza se observa em todos os fenômenos uma ordem natural. Assim, a eletricidade sempre flui do ponto de maior potencial para outro mais baixo. A água se move de um ponto mais alto para outro mais baixo. A difusão acontece de pontos de maior concentração para outro de menor concentração e todas as reações químicas acontecem na direção que leva a um ponto de melhor equilíbrio. Em resumo, todos os processos tendem a ir espontaneamente na direção que leva ao ponto de menor energia. Embora a primeira lei da termodinâmica estabeleça a relação entre calor absorvido e trabalho realizado por um sistema, este principio não estabelece nenhuma restrição com relação à fonte de calor ou da direção do fluxo de calor. Normalmente se associa a idéia de espontaneidade com uma diminuição de energia. Na química, isto acontece com as reações exotérmicas, que liberam calor para o meio, ou seja, após a reação o sistema tem menos energia que antes da reação. Mas esta condição por si só não é suficiente. Para exemplificar, veja-se a reação abaixo Ba(OH)2.8H2O(s) + 2NH4SCN(s) → Ba(SCN)2(s) + 2NH3 (g) + 10H2O(l) Esta reação absorve tanta energia do meio que chega a congelar a água resultante da reação. Por ser endotérmico, este sistema tem o seu conteúdo de energia aumentado, mas a reação é um processo claramente espontâneo. Conclui-se então, que a diminuição da energia não é uma condição suficiente para predizer se um processo é ou não espontâneo. Este fato demonstra que a primeira lei sozinha não consegue tratar sobre o assunto. O sentido da espontaneidade é dado pela segunda lei da termodinâmica. Para orientar o sentido das reações aplica-se o segundo princípio da termodinâmica. Este princípio define outra grandeza termodinâmica: a entropia. Para compreender melhor o conceito de entropia é melhor antes compreender um pouco de um ciclo termodinâmico clássico, ideal, conhecido pelo nome de ciclo de Carnot. Este ciclo é formado por quatro transformações ideais: duas transformações isotérmicas e duas adiabáticas como se mostra na figura abaixo. Com relação ao sentido de uma transformação, pode-se converter 100% do trabalho mecânico em calor, mas converter 100% do calor em trabalho útil é algo impossível de conseguir.
- 2. O trabalho total realizado neste ciclo contem quatro parcelas: Wtotal = W1 + W2 + W3 + W4 Aplicando a primeira lei da termodinâmica: 1. ÄU = Qentra – W1 O sistema absorve calor da fonte quente 2. ÄU = -W2 O sistema realiza trabalho 3. ÄU = Qsai – W3 O sistema libera o calor não transformado para a fonte fria 4. ÄU = W4 O sistema absorve trabalho Se o trabalho total for positivo (Wtotal > 0), então ele foi produzido à custa da energia térmica das vizinhanças. Condição necessária para se produzir trabalho. Devem existir duas fontes de calor. Uma quente e outra fria, de forma a ter um fluxo de calor da fonte quente para a fonte fria, passando por uma máquina térmica como mostra o sistema abaixo: Fonte quente Q1 Máquina W térmica Trabalho útil Q2 Fonte fria Equações: Rendimento de um ciclo térmico: É tido como a razão entre o trabalho útil obtido e o calor fornecido (Q1). Pode ser expresso também em percentual (%) W Q1 Mas W = Q1 – Q2 Q1 Q2 Então 1 2 Q Q1 Q1 Entretanto, medir calor é mais difícil que medir temperatura. Dispor de uma expressão que relaciona o rendimento com a temperatura simplifica a análise de um sistema. Sabe- se que Q = cp .ÄT. Substituindo-se essa expressão genérica em Q1 e Q2 obtem-se T1 T2 1 2 T T1 T1 Q1 é a fonte quente à temperatura T1 e Q2 é a fonte fria à temperatura T2
- 3. Entropia e a segunda lei da termodinâmica Se o rendimento térmico, ç, pode ser expresso tanto em termos de calor como de temperatura, então se pode igualar as expressões de forma que Q2 1 1 2 2 1 2 1 0 T Q Q Q Q Q1 T1 T2 T1 T2 T1 ou seja, somando todas as razões Q/T ao longo de um ciclo fechado, o resultado deve ser nulo para todos os processos reversíveis. Em termos diferenciais, fica 0 dQreversível T A integral com o círculo representa um ciclo fechado. A soma dos infinitos ciclos de Carnot que compõe o ciclo fechado representa que não há perda de calor durante o transcorrer de todo ciclo. Por definição esta integral fechada representa a grandeza termodinâmica conhecida pelo nome de entropia. Em termos físicos ela mede o grau de desordem do sistema. A unidade da entropia é J/(mol K) ou J/(g. K). A entropia como todas as demais propriedades termodinâmicas é uma propriedade de estado e depende somente dos estados inicial e final. Então, a variação de entropia de um sistema é medido como S S final S inicial Para sistemas reversíveis, a variação do calor do sistema em relação a sua temperatura é sempre nula. Para os ciclos não reversíveis, a integral resulta menor que zero, ou seja T 0 dQirreversível Significa que no ciclo houve uma perda de energia para o meio, de maneira que para se completar o ciclo é necessário um fornecer um pouco mais de energia, portanto a variação da entropia deve ser positiva, da qual resulta o enunciado da segunda lei da termodinâmica: Os processos termodinâmicos são espontâneos quando a variação da entropia resultar nula ou positiva. Se nula, o processo é considerado reversível, se positivo, é considerado irreversível, ou S sistema 0 Anotações de aula:
