Incorporar apresentação
Baixar para ler offline




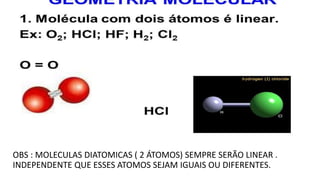

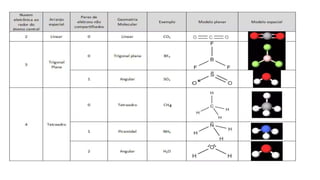

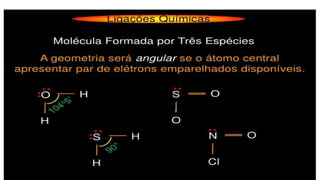
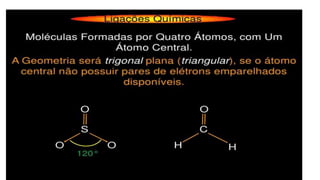
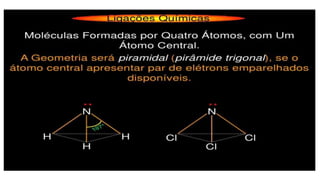
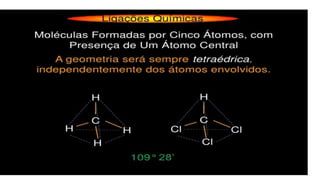
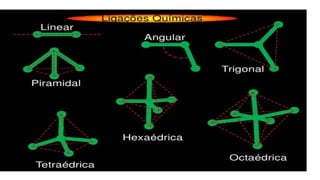







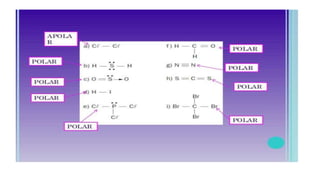



O documento discute moléculas diatômicas e como determinar a polaridade de moléculas. Moléculas diatômicas sempre serão lineares, independentemente dos átomos serem iguais ou diferentes. A polaridade de uma molécula depende do número de nuvens eletrônicas ao redor do átomo central em comparação com o número de grupos iguais ligados a esse átomo central. Se esses números forem iguais, a molécula será apolar; se forem diferentes, a molécula será polar. Exemplos específicos






















