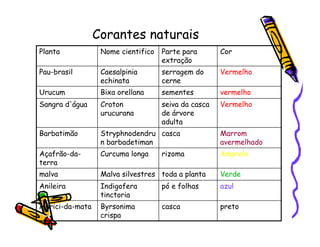
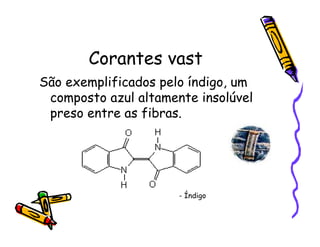
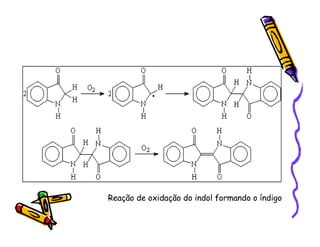
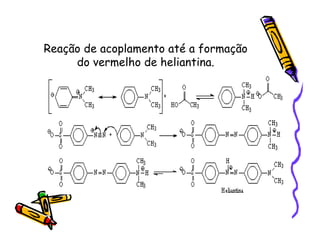
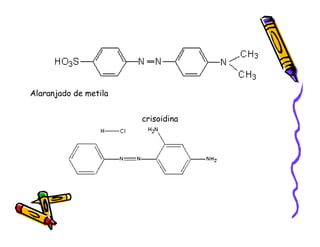
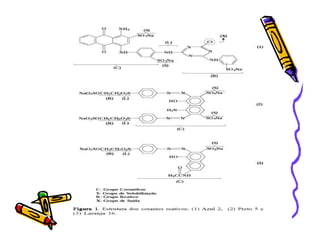
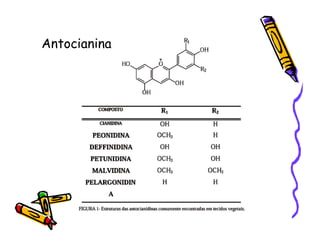
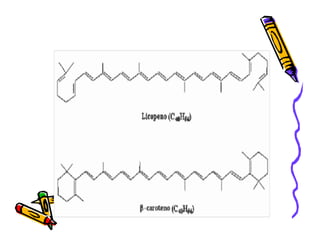
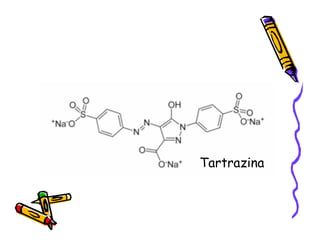
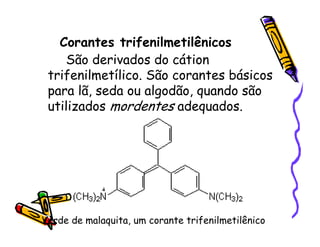
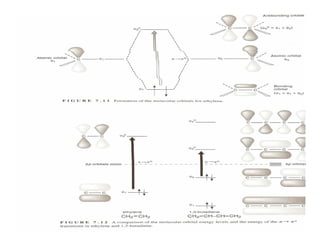
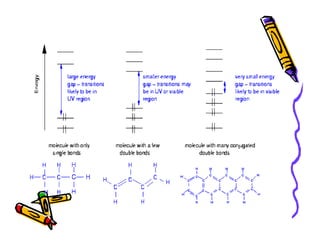
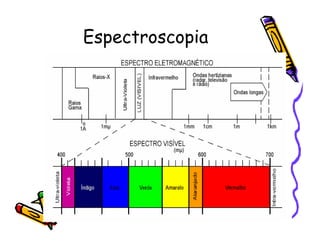
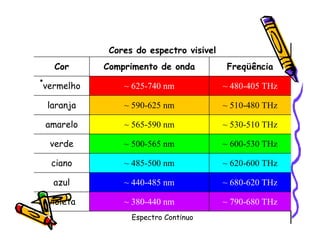
O documento discute a história e classificação de corantes naturais e sintéticos. Apresenta exemplos de corantes naturais extraídos de plantas e explica que os corantes sintéticos contêm grupos químicos chamados cromóforos responsáveis pela cor. Também descreve os principais tipos de corantes sintéticos e suas estruturas químicas.