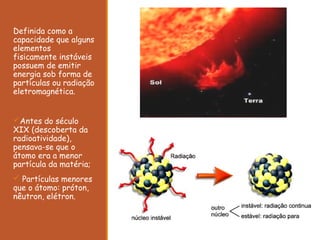
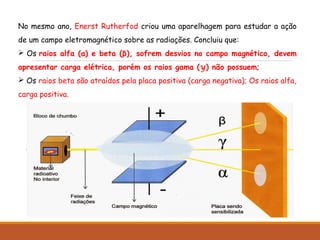
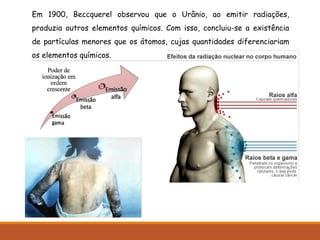
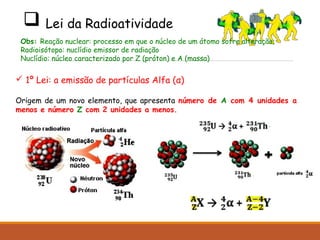
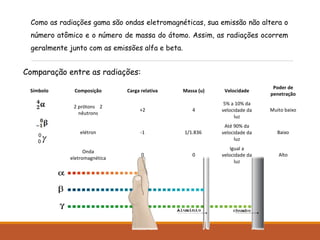
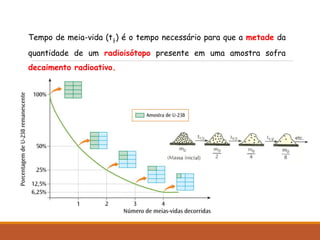
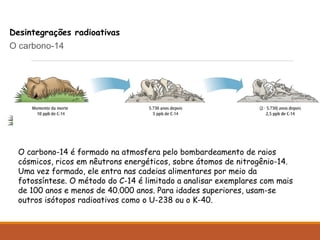
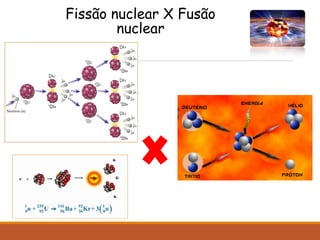
O documento descreve a descoberta da radioatividade no século 19 e as leis que regem o decaimento radioativo. Ele explica que a radioatividade envolve a emissão de partículas alfa, beta e raios gama e como cada tipo de emissão altera o núcleo atômico. Também discute as aplicações da radioatividade na medicina, agricultura, indústria e produção de energia nuclear.