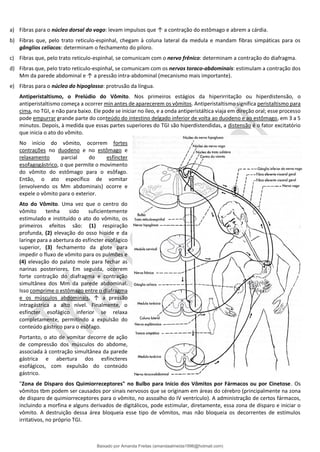
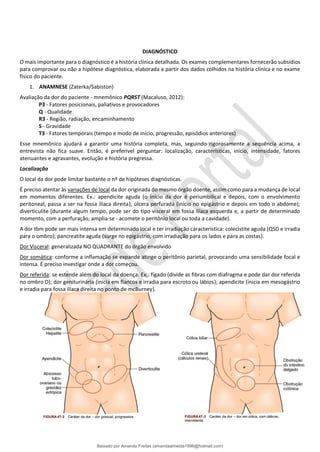
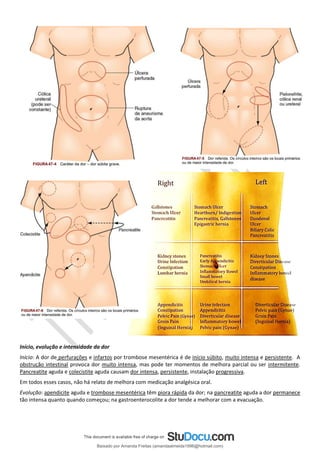
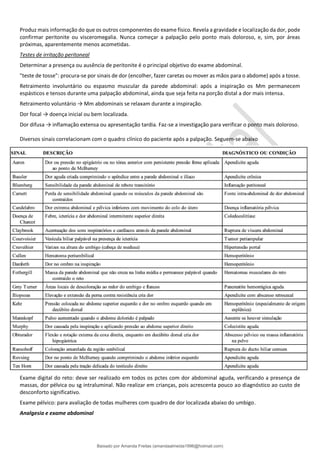
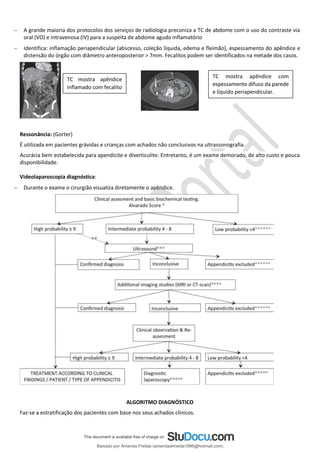
O documento fornece informações sobre a anatomia e fisiologia do sistema digestório e sobre as causas de dor abdominal aguda. Ele descreve as partes do estômago, duodeno, jejuno, íleo e intestino grosso, além de detalhar sua vascularização e inervação. Também explica os mecanismos de dor visceral, somática e referida no abdome. Por fim, categoriza as principais etiologias do abdome agudo.



































![• Tabagismo
− ↓a cicatrização
− prejudica a resposta à terapia
− ↑as complicações (perfuração)
− ↓produção de bicarbonato pelo duodeno proximal
− ↑risco de infecção pelo H. pylori
− gera radicais livres nocivos à mucosa.
O tabagismo pode predispor à doença ulcerosa péptica, mas a infecção por H. pylori continua sendo um fator de
confundimento não avaliado em estudos anteriores. O tabagismo não ↑o risco de ulceração recorrente se o H. pylori
for erradicado → tabagismo talvez seja um fator de risco apenas para os indivíduos infectados.
• Álcool
Papel ainda incerto. Álcool estimula a produção de HCl, a entrada de grandes [ ] na mucosa gástrica causa lesão direta.
Acredita-se que o risco seja maior em pacientes infectados com H. pylori.
• Estresse emocional
Os pctes vítimas de choque, sepse, queimaduras extensas, traumatismo grave ou lesão podem desenvolver alterações
mucosas de gastrite erosiva aguda ou ulceração franca com sangramento.
• Gastrinoma com/sem síndrome de neoplasia endócrina múltipla tipo 1
Tumores secretores de gastrina: importante causa de hipersecreção gástrica (impulso mantido para secreção de ác).
Pode resultar em múltiplas ulcerações no estômago e no duodeno, refratárias ao tto convencional e muitas vezes
associada a diarreia crônica.
• Transtornos Diversos
Doença de Crohn: pode causar ulcerações em qualquer parte do TGI.
Deficiência de α1-antitripsina, doença pulmonar crônica e insuficiência renal crônica: podem causar úlceras pépticas.
• Doença de Ménétrier - rara, hiperplasia das céls mucosas superficiais e glandulares, que substitui a maior
parte das céls principais e parietais (↓HCl). Pode vir acompanhada de náuseas, vômitos, sangramento.
DIAGNÓSTICO DIFERENCIAL
A lista de distúrbios gastrintestinais e não gastrintestinais que podem simular uma ulceração do estômago ou do
duodeno é bastante extensa. O principal deles é a dispepsia sem úlcera (DSU).
Vários outros processos patológicos que podem manifestar-se com sintomas "semelhantes aos da úlcera” incluem
tumores GI proximais, refluxo gastresofágico, doença vascular, doença pancreatobiliar (cólica biliar, pancreatite
crônica) e doença de Crohn gastroduodenal.
MANIFESTAÇÕES CLÍNICAS
• Anamnese
Os sintomas referidos pelos pctes não permitem diferenciar úlcera duodenal (UD) e úlcera gástrica (UG) e podem ser
muito discretos, atípicos ou ausentes. Quando presente, a costuma ser dor pouco intensa, em queimação, no
epigástrio, circunscrita e descrita como “dor de fome, queimadura ou desconforto na boca do estômago”.
A dor mantém-se por semanas, de forma rítmica. A ritmicidade é relação íntima da dor com a alimentação:
− Úlcera duodenal: melhora da dor com a ingestão de alimentos (chamada de dor em 3 tempos: dói-come-passa);
− Úlcera gástrica: ingestão de alimentos às vezes piora ou desencadeia a dor (dor em 4 tempos: dói-come-passa-dói).
Outra característica da dor é a periodicidade: períodos de acalmia (desaparecimento da dor por meses ou anos)
intercalados por outros sintomáticos. O fato de o paciente ser despertado pela dor no meio da noite (clocking) é
sugestivo da presença de úlcera, particularmente, duodenal.
A pirose ou azia é comum nos pacientes com UD, em virtude da associação da UD com refluxo gastresofágico. Outros
sintomas dispépticos, como eructação, flatulência, sialorreia, náuseas e vômitos, não são próprios da úlcera péptica,
mas podem estar associados.
NOTA: Em pacientes com doença ulcerosa relacionada aos AINEs, a dor muitas vezes está ausente. Assim, os sintomas
clássicos não são sensíveis nem específicos da doença ulcerosa.
• Exame físico
Baixado por Amanda Freitas (amandaalmeida1996@hotmail.com)
lOMoARcPSD|5059377](https://image.slidesharecdn.com/modulo-dor-abdominal-resumo-medicina-200630162919/85/Modulo-dor-abdominal-resumo-medicina-48-320.jpg)

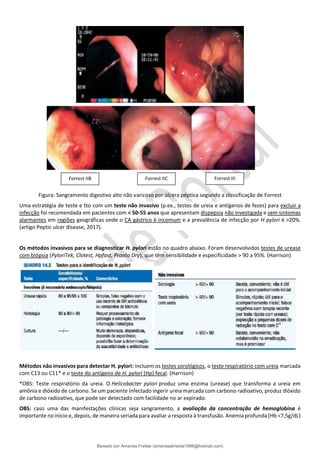






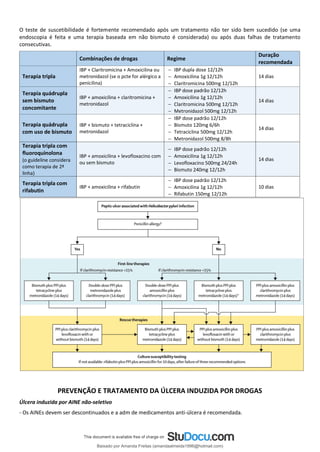














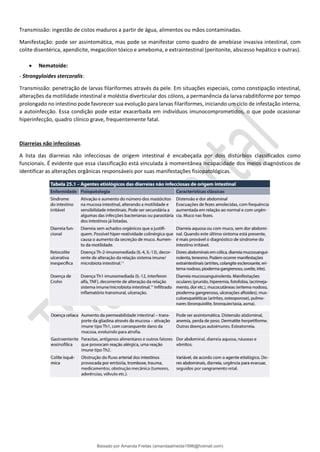
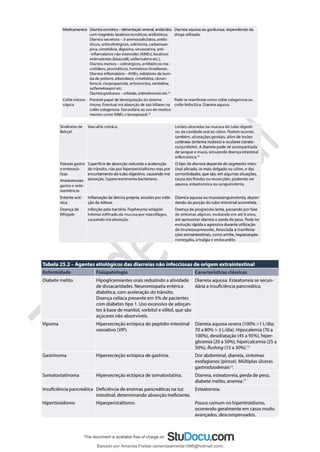










































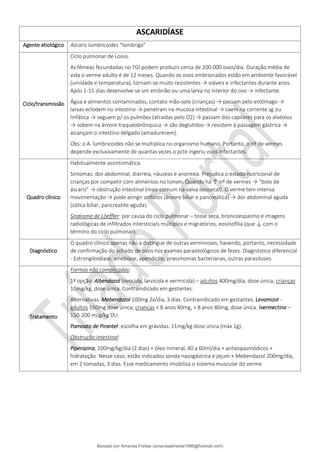
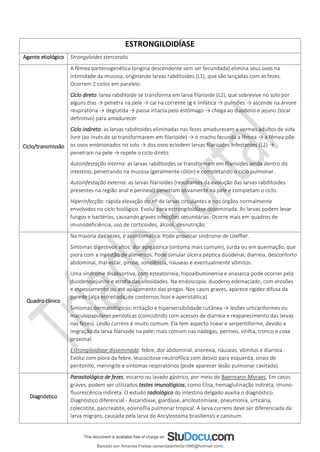
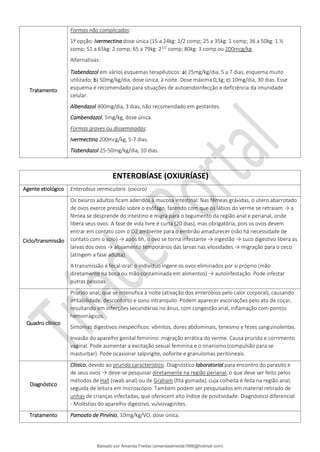
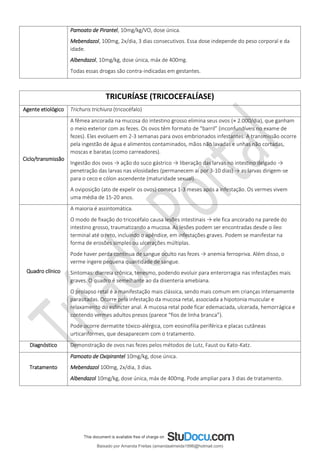





















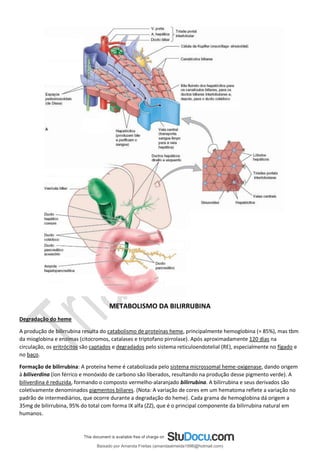
![Transporte plasmático: a bilirrubina lançada na circulação, na forma não conjugada ou “indireta”, liga-se à
albumina, sendo por ela transportada (pois ela é pouco solúvel). Cada molécula de albumina tem 2 sítios de ligação
com a bilirrubina, mas caracteristicamente a 1ª ligação é até 300x mais forte do que a 2ª. (Nota: Certas drogas
aniônicas, como salicilatos e sulfonamidas, podem deslocar a bilirrubina da albumina, permitindo que a bilirrubina
penetre no sistema nervoso central [SNC]. Esse fenômeno é potencialmente causador de lesão nervosa nos bebês).
Captação da bilirrubina pelo fígado: A bilirrubina dissocia-se da albumina e entra no hepatócito, onde se liga a
proteínas intracelulares, especialmente à proteína ligandina (proteína Y) e, em menor escala, com a proteína Z.
Conjugação: Para ser excretada, a bilirrubina indireta precisa ser transformada em produtos mais solúveis. Em seres
humanos, esse processo se realiza pela conjugação da molécula de bilirrubina com o ácido glicurônico, no
hepatócito (através da adição de duas moléculas de ácido glicurônico), dando origem à bilirrubina conjugada ou
“direta”, que na verdade é um diglicuronídio de bilirrubina. Essa reação é catalisada por 2 enzimas:
glicuroniltransferase (que catalisa a conjugação da bilirrubina para monoglicuronídio de bilirrubina) e uma
transferase associada à membrana (MGt – que catalisa a reação de 2 moles de monoglicuronídio de bilirrubina,
dando origem a um mol de diglicuronídio de bilirrubina e a um mol de bilirrubina não conjugada, que volta ao
retículo endoplasmático para nova conjugação).
Excreção da bilirrubina na bile: após a conjugação, o diglicuronato de bilirrubina é transportado ativamente contra
um gradiente de concentração para ser excretado na rede biliar e, em seguida, para a luz do TGI. Esse passo
dependente de energia é limitante da velocidade e suscetível a prejuízo em casos de doença hepática. A bilirrubina
não-conjugada normalmente não é excretada.
Formação de urobilinas no intestino. O diglicuronato de bilirrubina é hidrolisado e reduzido por bactérias no
intestino, produzindo urobilinogênio, um composto incolor. A maior parte do urobilinogênio é oxidada, por
bactérias intestinais, a estercobilina, que dá às fezes sua cor marrom característica. No entanto, uma parte do
urobilinogênio é reabsorvida no intestino e entra no sg pelo sistema porta e participa do ciclo entero-hepático do
urobilinogênio → ele é captado pelo fígado e novamente excretado na bile. O restante do urobilinogênio é
transportado pelo sg para o rim, onde é convertido em urobilina, que é amarela e que, ao ser excretada, dá à urina
sua cor característica.
Baixado por Amanda Freitas (amandaalmeida1996@hotmail.com)
lOMoARcPSD|5059377](https://image.slidesharecdn.com/modulo-dor-abdominal-resumo-medicina-200630162919/85/Modulo-dor-abdominal-resumo-medicina-149-320.jpg)












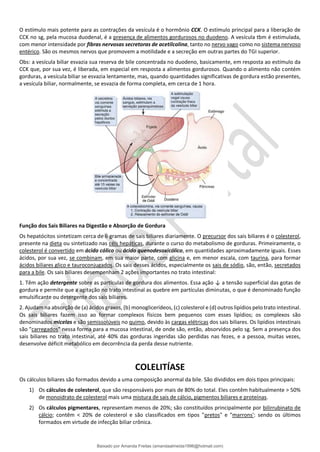


![DIAGNÓSTICO (Harrison)
A ultrassonografia da vesícula biliar é muito precisa na identificação da colelitíase. Cálculos com apenas 2 mm de
diâmetro podem ser identificados de forma confiável, desde que sejam utilizados critérios rígidos [p. ex., "sombreado"
acústico de opacidades que estão dentro do lúmen vesicular e que se modificam com a posição do paciente (pela
gravidade)]. A lama biliar é representada por um material com baixa atividade ecogênica que forma uma camada na
posição mais baixa da vesícula biliar. Tal camada se desloca com as mudanças posturais, porém não produz sombreado
acústico; essas duas características distinguem a lama dos cálculos biliares. A ultrassonografia pode ser também usada
para determinar a função de esvaziamento da vesícula biliar.
A radiografia simples de abdome pode detectar os cálculos biliares que contêm quantidades suficientes de cálcio a
ponto de se tornarem radiopacos (10 a 15% de colesterol e cerca de 50% de cálculos pigmentares). Também pode ser
usada para fazer o diagnóstico de colecistite enfisematosa, vesícula de porcelana, bile calcificada e íleo biliar.
O colecistograma oral (CGO) é considerado como obsoleto. Pode ser usado para determinar a permeabilidade do
ducto cístico e a função de esvaziamento da vesícula biliar. Além disso, o CGO pode delinear o tamanho e nº de cálculos
biliares, bem como determinar se estão calcificados.
TRATAMENTO
Tratamento cirúrgico
Nos pctes assintomáticos, o risco de desenvolver sintomas ou complicações que tornem necessária uma cirurgia é
bastante pequeno (1 a 2% ao ano). Recomendação para colecistectomia deve basear-se na avaliação de três fatores:
(1) presença de sintomas suficientemente frequentes ou intensos a ponto de interferir na rotina geral do pcte; (2)
presença de complicação prévia da doença calculosa biliar (história de colecistite aguda, pancreatite, fístula biliar); ou
(3) presença de condição subjacente que predisponha o pcte a ↑ risco de complicações devidas aos cálculos (p. ex.,
vesícula biliar calcificada ou de porcelana, ataque prévio de colecistite aguda não obstante o atual estado
assintomático).
− Pctes com cálculos biliares muito volumosos (> 3 cm de diâmetro) e os com cálculos em vesícula biliar com alguma
anomalia congênita tbm podem ser aventados para ser submetidos a uma colecistectomia profilática.
− A idade jovem é fator preocupante nos pctes com cálculos biliares assintomáticos, porém poucos autores
recomendam atualmente colecistectomia de rotina em todos os pacientes jovens com cálculos silenciosos.
A colecistectomia laparoscópica é uma abordagem de acesso mínimo para a retirada da vesícula biliar juntamente
com seus cálculos. Vantagens: ↓ da permanência no hospital, incapacitação mínima e ↓custo, sendo o procedimento
de escolha na maioria dos pctes encaminhados a uma colecistectomia eletiva.
Terapia clínica – dissolução dos cálculos biliares
Baixado por Amanda Freitas (amandaalmeida1996@hotmail.com)
lOMoARcPSD|5059377](https://image.slidesharecdn.com/modulo-dor-abdominal-resumo-medicina-200630162919/85/Modulo-dor-abdominal-resumo-medicina-168-320.jpg)

![− O pcte apresenta-se anorético e nauseado.
− Os vômitos são comuns, podendo produzir sintomas e sinais de depleção volêmica vascular e extravascular.
− A icterícia é incomum no início da evolução da colecistite aguda, mas pode ocorrer quando as alterações
inflamatórias edematosas acometem os ductos biliares e linfonodos circundantes.
− A febre é baixa, porém os calafrios com agitação ou os arrepios não são incomuns.
− O QSD do abdome apresenta-se quase invariavelmente hipersensível à palpação. Uma vesícula biliar tensa e
aumentada de volume é palpável em 25 a 50% dos pctes.
− A respiração profunda ou tosse durante a palpação subcostal do QSD produz habitualmente ↑da dor e parada
inspiratória (sinal de Murphy). A descompressão dolorosa com hipersensibilidade localizada no QSD é comum, o
mesmo ocorrendo com distensão abdominal e ruídos intestinais hipoativos em virtude do íleo paralítico, porém
geralmente faltam sinais peritoniais generalizados e rigidez abdominal na ausência de perfuração.
DIAGNÓSTICO (Harrison)
Anamnese característica e um bom exame físico. A tríade de 1) início súbito de hipersensibilidade no QSD 2) febre e
3) leucocitose é altamente sugestiva.
− A leucocitose fica entre 10.000 e 15.000 céls por microlitro com um desvio para a E na contagem diferencial.
− A bilirrubina sérica torna-se levemente ↑ [< 85,5 μ.mol/L (5 mg/dL)] em menos da metade dos pctes, enquanto
cerca de 25% evidenciam ↑moderadas das aminotransferases séricas (em geral, elevação < 5x).
− O US demonstra a presença de cálculos em 90 a 95% dos casos, sendo útil na identificação dos sinais de
inflamação da vesícula (espessamento da parede, líquido pericolecístico e dilatação do ducto biliar).
− A cintilografia biliar com radionuclídio (p. ex., HIDA) poderá confirmar o diagnóstico se for visualizada a imagem
do ducto biliar sem a visualização da vesícula biliar.
OBS: A síndrome de Mirizzi é uma complicação rara na qual um cálculo biliar fica impactado no ducto cístico ou colo
da vesícula biliar, causando compressão do colédoco, resultando em obstrução coledociana e icterícia. O US mostra
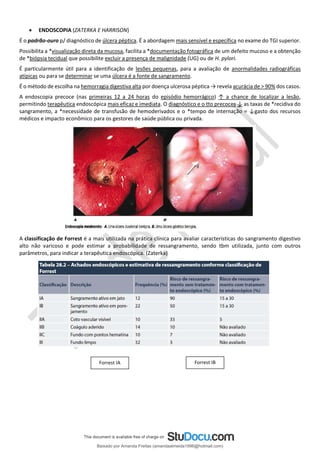
cálculo(s) biliar(es) fora do ducto hepático. A colangiopancreatografia retrógrada endoscópica (CPRE) (Fig. 45.2B) ou
a colangiografia transepática percutânea (CTP) ou a colangiopancreatografia por ressonância magnética (CPRM)
demonstram habitualmente a compressão extrínseca característica do colédoco. A cirurgia consiste em remover o
ducto cístico, a vesícula biliar enferma e o cálculo impactado. O diagnóstico pré-operatório da síndrome de Mirizzi é
importante para evitar uma lesão do colédoco.
CLASSIFICAÇÃO DAS COLECISTITES (Harrison e Dani)
1) Colecistite Aguda Calculosa (CAC)
Etiologia
É uma complicação da litíase biliar e depende da obstrução do canal cístico por um ou mais cálculos biliares.
Fisiopatologia
A migração de cálculo(s) da vesícula para o infundíbulo vesicular, para o cístico ou para o colédoco pode provocar
uma obstrução. Se esta não é aliviada, há ↑ da pressão intraluminal e distensão da vesícula. Isso provoca os
Baixado por Amanda Freitas (amandaalmeida1996@hotmail.com)
lOMoARcPSD|5059377](https://image.slidesharecdn.com/modulo-dor-abdominal-resumo-medicina-200630162919/85/Modulo-dor-abdominal-resumo-medicina-170-320.jpg)