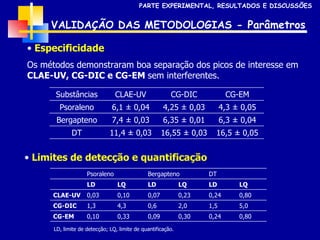
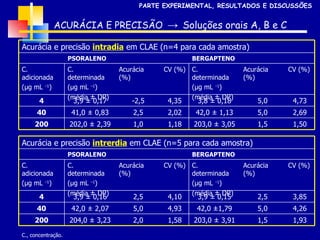
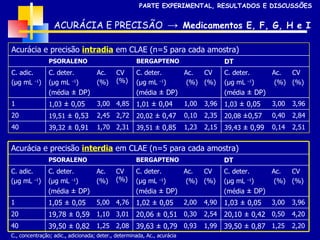
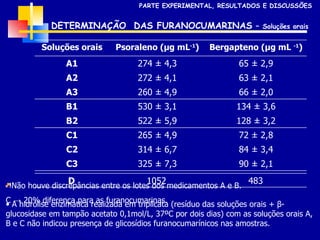
1) O documento descreve o desenvolvimento e validação de metodologias para determinação de furanocumarinas em medicamentos fitoterápicos.
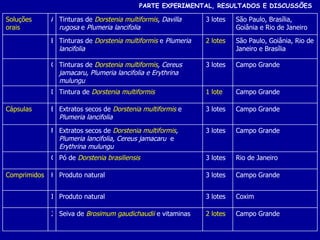
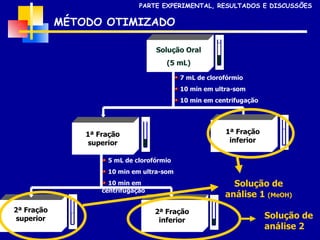
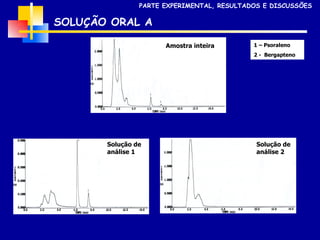
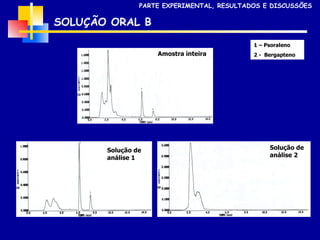
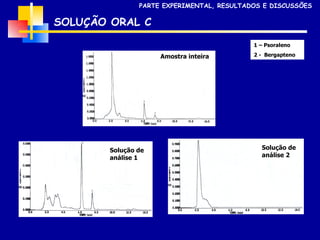
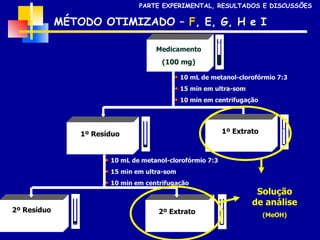
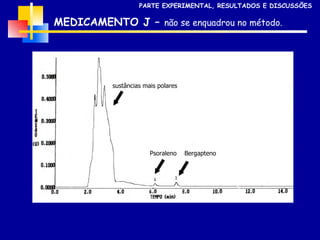
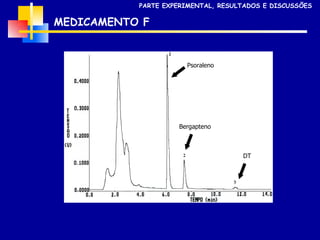
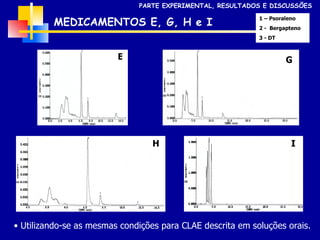
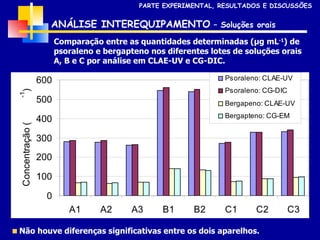
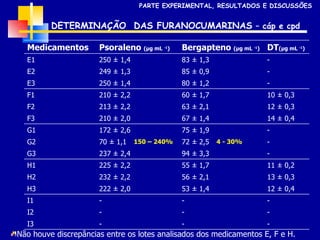
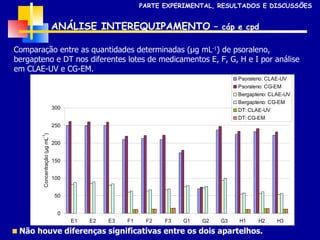
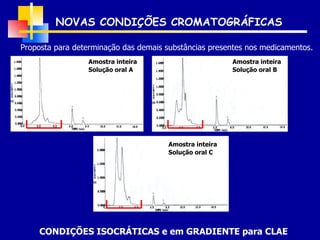
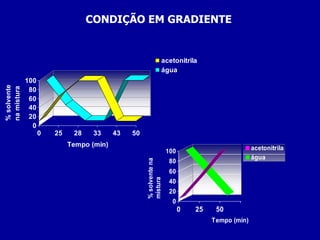
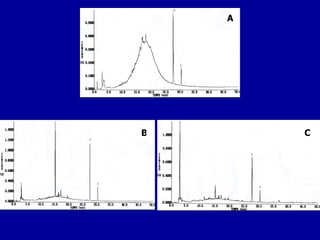
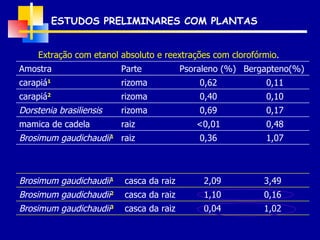
2) Foram analisados 10 medicamentos obtidos no comércio e desenvolvidos métodos de extração e cromatografia para identificar furanocumarinas.
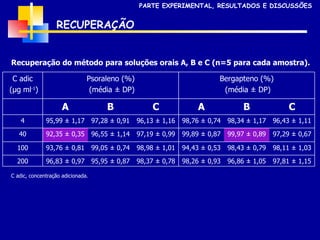
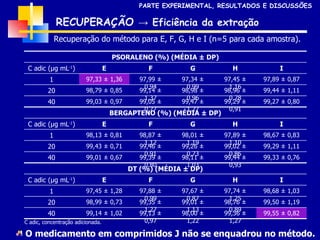
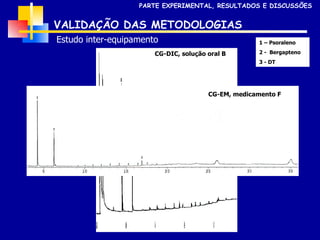
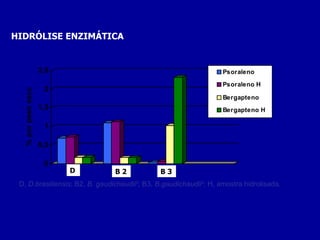
3) Os métodos desenvolvidos foram validados de acordo com parâmetros internacionais e forneceram resultados precisos e recuperações adequadas para as amostras analisadas.






![FURANOCUMARINAS OU PSORALENOS Famílias Apiaceae, Rutaceae e Moraceae . INTRODUÇÃO * 5-[3-(4,5-Diidro-5,5-dimetil-4-oxo-2-furanil)-butoxi]-7H-furo[3-2-g][1]benzopiran-7-ona *](https://image.slidesharecdn.com/apresentaomestradofinal-090912175421-phpapp01/85/Minha-defesa-de-dissertacao-2004-8-320.jpg)