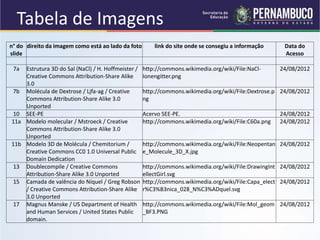
O documento discute os tipos de ligação química, com foco na ligação covalente. Explica como a formação de ligações químicas entre átomos resulta em uma diminuição de energia do sistema à medida que forças de atração superam as de repulsão. Também descreve os conceitos de valência, potencial de ionização, afinidade eletrônica e polaridade de ligações.