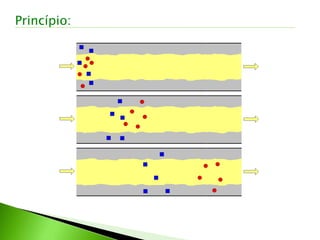
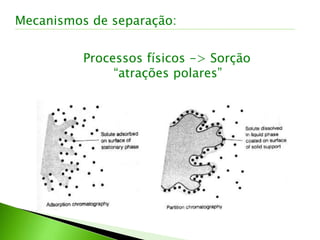
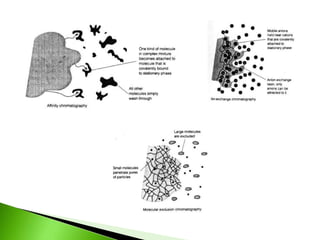
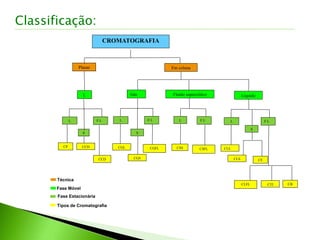
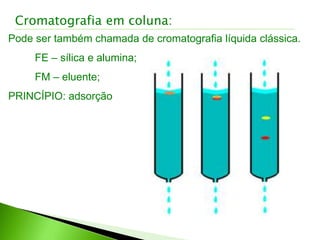
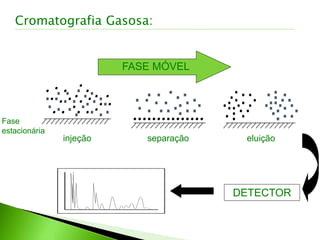
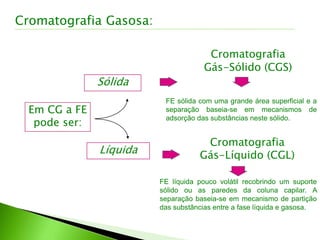
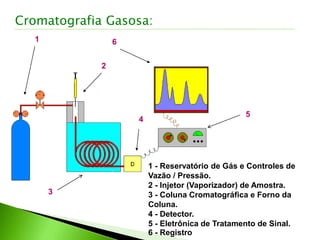
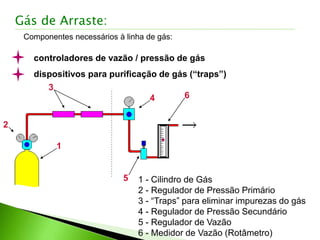
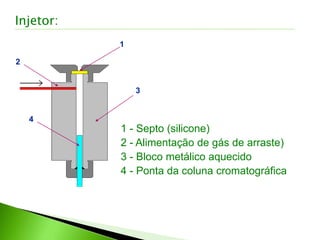
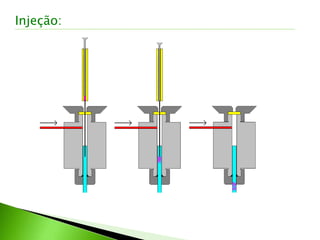
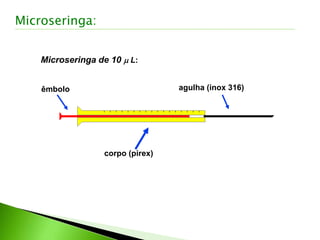
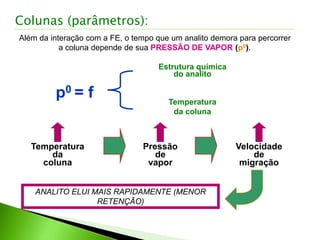
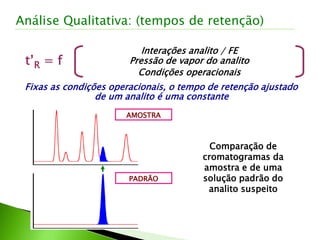
O documento descreve os principais conceitos e técnicas de cromatografia. A cromatografia é um método de separação de componentes de uma mistura por meio da interação entre uma fase estacionária e uma fase móvel. As principais técnicas descritas incluem cromatografia gasosa, cromatografia líquida, cromatografia em camada delgada e cromatografia em papel. Detectores comuns como detector por ionização em chama e detector por condutividade térmica também são abordados.


![Histórico:
M. TSWEET (1903): Separação de misturas de
pigmentos vegetais em colunas recheadas com
adsorventes sólidos e solventes variados.
éter de
petróleo
CaCO3
mistura de
pigmentos
pigmentos
separados
Cromatografia =
kroma [cor] + graph [escrever]
(grego)](https://image.slidesharecdn.com/cromatografiaaula-140827092133-phpapp02/85/Cromatografia-aula-3-320.jpg)