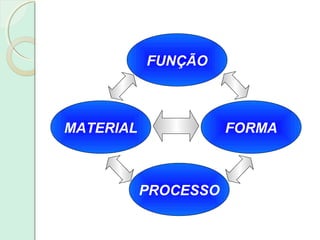
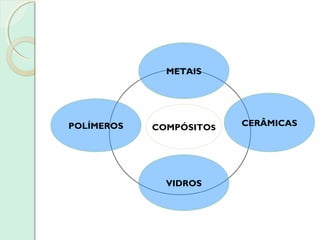
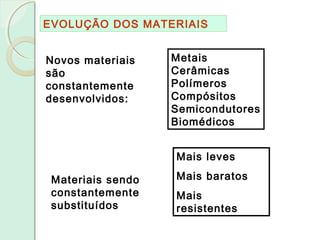
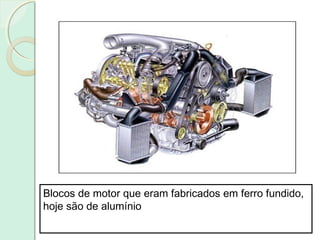
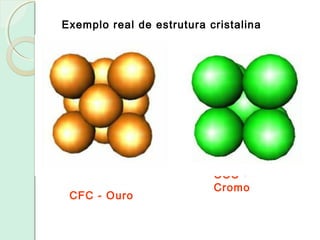
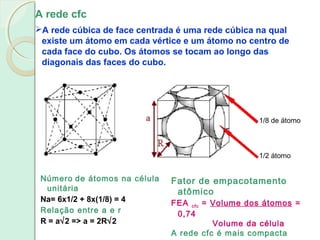
Este documento apresenta um plano de curso para a disciplina Introdução à Ciência dos Materiais. O curso abordará as propriedades mecânicas e diagramas de fases dos materiais, com o objetivo de compreender as características físicas e estruturais de materiais metálicos, plásticos e cerâmicos. Serão discutidas unidades sobre estrutura atômica, diagramas de fase e deformação dos materiais.