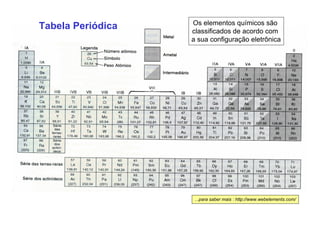
1. O documento discute classificação de materiais e tipos de ligação química.
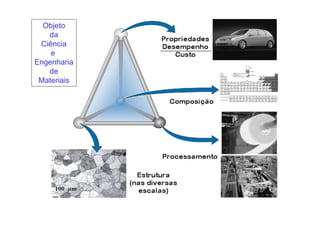
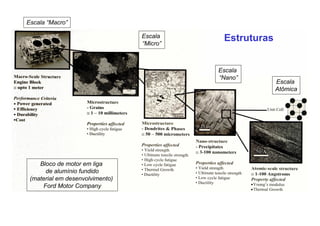
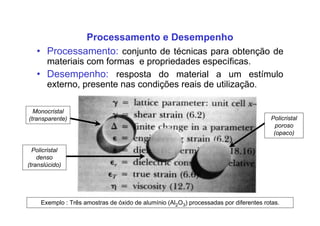
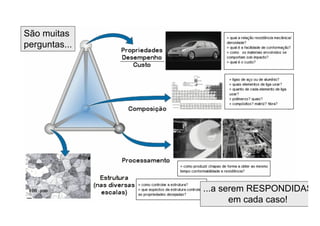
2. São apresentadas definições de ciência e engenharia de materiais e como composição, estrutura e processamento afetam propriedades.
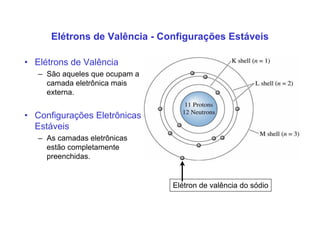
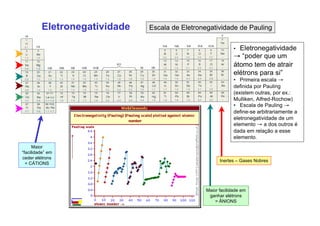
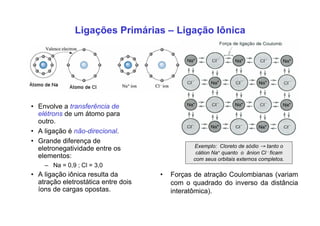
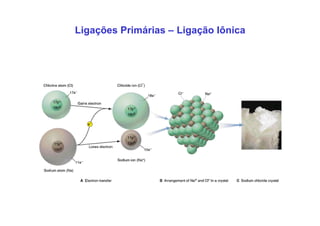
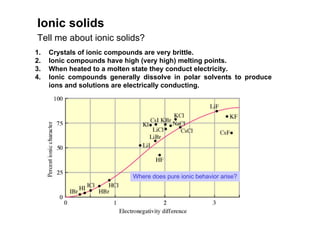
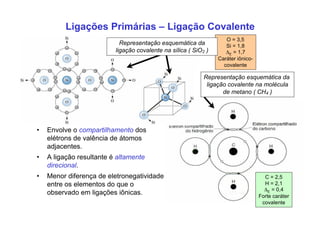
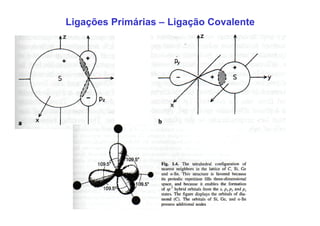
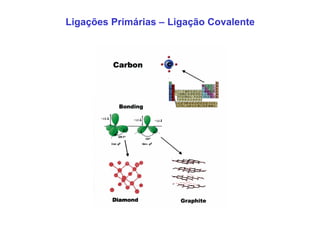
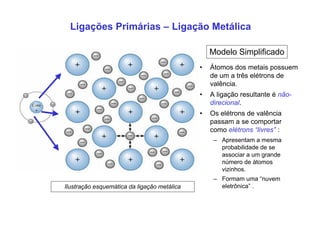
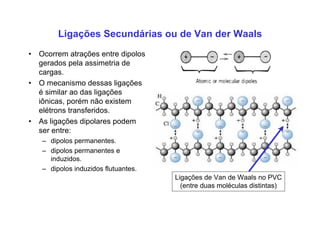
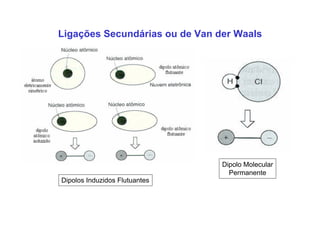
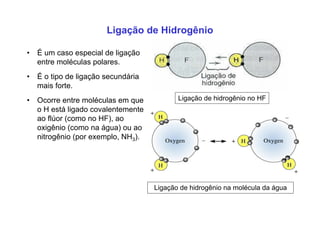
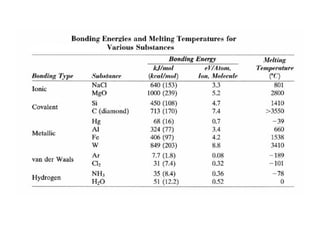
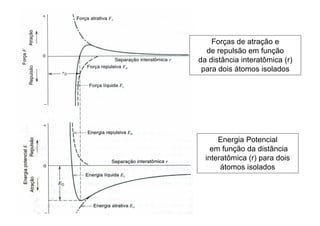
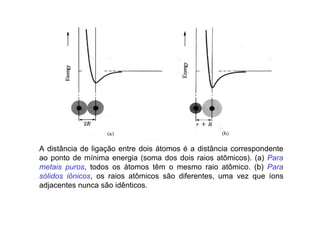
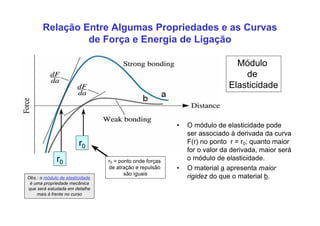
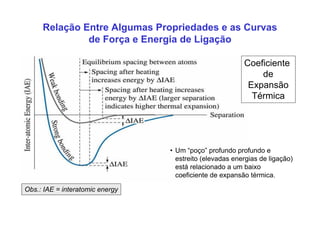
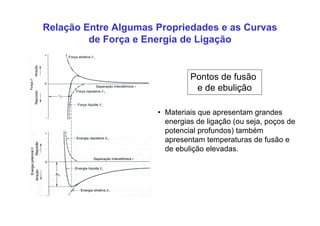
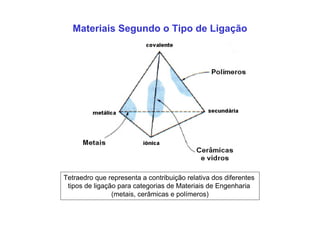
3. São descritos tipos de ligação química como iônica, covalente e metálica e como elas influenciam propriedades dos materiais.