O documento discute o sistema de liberação de fármacos (Drug Delivery) utilizando nanocarrregadores. Aborda os tipos de nanocarrregadores, métodos de preparo, vias de administração e aplicações, especialmente no tratamento do câncer, utilizando alvos como o Efeito Enhanced Permeability and Retention (EPR).


![[1]](https://image.slidesharecdn.com/apresentao-drugdeliveryfinal-130806224430-phpapp02/85/Drug-Delivery-3-320.jpg)
![Figura 2 – Países com a maior prevalência de Diabetes [1].](https://image.slidesharecdn.com/apresentao-drugdeliveryfinal-130806224430-phpapp02/85/Drug-Delivery-4-320.jpg)
![Figura 3 – Ilhotas de Langerhans [2].
O sistema imunológico do
paciente destrói progressivamente
as células Beta, responsáveis pela
produção da insulina.](https://image.slidesharecdn.com/apresentao-drugdeliveryfinal-130806224430-phpapp02/85/Drug-Delivery-5-320.jpg)
![Diabetes Tipo 2
[glicemia]
Tempo
70 -
120 -
Figura 4 – Em preto mostra a variação da glicemia de uma pessoa saudável,
enquanto em laranja mostra o nível de glicemia em pessoas que sobrecarregam o
organismo com carboidratos](https://image.slidesharecdn.com/apresentao-drugdeliveryfinal-130806224430-phpapp02/85/Drug-Delivery-6-320.jpg)
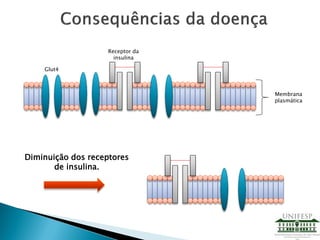
![Liberação de
insulina, devido
a falência das
células Beta
Figura 5 – Pâncreas [3].](https://image.slidesharecdn.com/apresentao-drugdeliveryfinal-130806224430-phpapp02/85/Drug-Delivery-8-320.jpg)
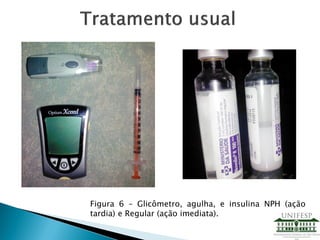
![Figura 7 – Aplicação da insulina [4]
Dependendo do avanço e tratamento da Diabetes, é
necessária a aplicação intravenosa de 4 a 6 vezes ao
dia.](https://image.slidesharecdn.com/apresentao-drugdeliveryfinal-130806224430-phpapp02/85/Drug-Delivery-10-320.jpg)
![Figura 8 – Uma solução
seria “tomar” a insulina,
mas será que é possível a
insulina ser administrada
oralmente e manter suas
propriedades bioquímicas?
Infelizmente não, pois é
um hormônio proteico e
seria metabolizada no TGI.
[5].](https://image.slidesharecdn.com/apresentao-drugdeliveryfinal-130806224430-phpapp02/85/Drug-Delivery-11-320.jpg)

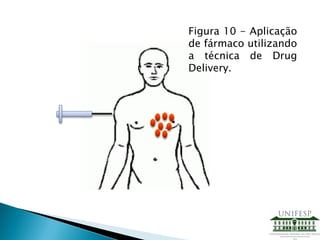

![Figura 11 – Exemplos de Carriers utilizados no sistema de Drug Delivery [7].](https://image.slidesharecdn.com/apresentao-drugdeliveryfinal-130806224430-phpapp02/85/Drug-Delivery-17-320.jpg)
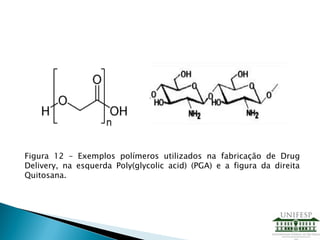
![Requisitos para uso de Drug Carriers
Biocompatibilidade Biofuncionalidade
Não tóxico Física Fácil manuseio
Não Carcinogênico Química Não incomodo ao
paciente
Não imunogênico Mecânica
Não trombogênico Térmica
Reabsorvível
Tabela 1 – Principais caracteristicas para utilização de Drug Carriers [8].](https://image.slidesharecdn.com/apresentao-drugdeliveryfinal-130806224430-phpapp02/85/Drug-Delivery-19-320.jpg)


![Vantagens: Fácil manuseio,
barato, seguro, diferentes
doses podem ser
ministradas.
Desvantagens: Baixa
absorção comparado a
outros métodos, o paciente
pode estar impossibilitado
(glote inchada).
Figura 13 – Administração via
oral [9].](https://image.slidesharecdn.com/apresentao-drugdeliveryfinal-130806224430-phpapp02/85/Drug-Delivery-22-320.jpg)
![Figura 14 – Administração bocal de Drug
Delivery [8].
Vantagens:
• Rápida absorção;
• No Liver (metabolismo
de 1° passagem e Sistema Porta
Hepática);
• pH salivar neutro;
Desvantagens:
• Incomodo;
• Drogas em testes;](https://image.slidesharecdn.com/apresentao-drugdeliveryfinal-130806224430-phpapp02/85/Drug-Delivery-23-320.jpg)
![Figura 15 – Administração ocular,
método conhecido como Ocular
Iontophoresis [10].
Vantagens:
• Rápida absorção;
Desvantagens:
• Processo que exige
pessoas qualificadas;
• Caro, pois utiliza
anestesia local;](https://image.slidesharecdn.com/apresentao-drugdeliveryfinal-130806224430-phpapp02/85/Drug-Delivery-24-320.jpg)
![Figura 16 – Administração via nasal [8].
Vantagens:
• Rápida absorção;
Desvantagens:
• Fagocitose pelos
macrófagos alveolares;](https://image.slidesharecdn.com/apresentao-drugdeliveryfinal-130806224430-phpapp02/85/Drug-Delivery-25-320.jpg)
![Figura 17 – Administração parental, pode ser intramuscular,
subcutânea ou intravenosa [8].](https://image.slidesharecdn.com/apresentao-drugdeliveryfinal-130806224430-phpapp02/85/Drug-Delivery-26-320.jpg)

![Figura 18 – Administração
epitelial [8].
Vantagens:
• Fácil manuseio;
Desvantagens:
• Absorção lenta;
• Pode causar irritação;](https://image.slidesharecdn.com/apresentao-drugdeliveryfinal-130806224430-phpapp02/85/Drug-Delivery-28-320.jpg)
![Figura 19 – Representação de método de preparo
de nanopartículas por dispersão (Solvent
displacement ). [11].
• Diversos métodos;
O fármaco geralmente é
assimilado ao Carrier
durante o processo de
fabricação, porém pode
sofrer avarias ocasionado
por:
• Temperatura
• Pressão
• Agitação](https://image.slidesharecdn.com/apresentao-drugdeliveryfinal-130806224430-phpapp02/85/Drug-Delivery-29-320.jpg)
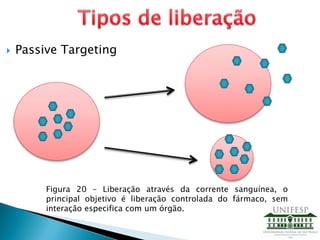
![ Active Targeting
Figura 21 – Right
Kidney, em azul
está representado
os receptores
específicos que
permitem a
interação do Drug
Carrier com o
órgão, ou seja,
liberação controlada
e local [12].](https://image.slidesharecdn.com/apresentao-drugdeliveryfinal-130806224430-phpapp02/85/Drug-Delivery-31-320.jpg)


![Figura 22 – Representação do EPR – Effect [13].](https://image.slidesharecdn.com/apresentao-drugdeliveryfinal-130806224430-phpapp02/85/Drug-Delivery-34-320.jpg)

![Dificuldades
Tamanho;
Estabilidade, estrutura delicada;
Enzimas e substâncias de degradação;
Solução
Incluindo a modificação química;
co-administração com promotores de absorção
e/ou inibidores de enzimas;
Dispositivos de liberação controlada –
carregadores [15];](https://image.slidesharecdn.com/apresentao-drugdeliveryfinal-130806224430-phpapp02/85/Drug-Delivery-36-320.jpg)
![ Nanopartículas poliméricas – nanoesferas e
nanocápsulas;
Nanovesículas;
Nanopartículas lipídicas sólidas;
Figura 23: Tipos de nanocarregadores [7]](https://image.slidesharecdn.com/apresentao-drugdeliveryfinal-130806224430-phpapp02/85/Drug-Delivery-37-320.jpg)





![Nanopartículas magnéticas como nanovetores
de liberação de drogas com os lipossomos.
Figura 24: Nanoparticulas magnéticas [14].](https://image.slidesharecdn.com/apresentao-drugdeliveryfinal-130806224430-phpapp02/85/Drug-Delivery-43-320.jpg)



![ [1] – International Diabetes Federation , 2009.
[2] - farmaciaminhavida.blogspot.com.br/2013/03/tipos-de-hormonios-insulina-
glucagon
[3] - atlas.centralx.com.br/p/imagem/sistema-digestorio/pancreas/
[4] - www.mundodastribos.com/diabetes-tipo-1-sintomas
[5] - www.terrazul.com.br/avaliacaofisica/perca-peso-tomando-agua/
[6] - fazendoaminhafestacolorir.blogspot.com.br/2012/05/corpo-humano-
imagens-para-colorir
[7] – JYOTHIRMAI C., MOBINA M.; An overview na Drug Delivey to the brain – St.
Mary’s College of Pharmacy. Disponível em:
www.authorstream.com/Presentation/aSGuest130588-1371258-drug-delivery/
[8] - ADAM M. K.; Drug Deleivery – Larpm. Disponível em:
www.authorstream.com/Presentation/neetaTanajiJare-1070247-microspheres-
drug-delivery-system/](https://image.slidesharecdn.com/apresentao-drugdeliveryfinal-130806224430-phpapp02/85/Drug-Delivery-47-320.jpg)
![ [9] - paraisomodabebe.com.br/blog/ze-gotinha/
[10] – SUJIT R. P.; Ocular Drug Delevery System - Maratha Mandal College of
Pharmacy. Disponível em: www.slideshare.net/sujitpatel11/ocular-drug-
delivery-system
[11] - HENELYTA S. R., BOON-SEANG C., SOSAKU I., MITSUTOSHI N.;
Preparation of nanodispersions containing β-carotene by solvent
displacement method; Food Hydrocolloides – 2008.
[12] - KUMAR V. S.; Kidney Cancer – Risks, Symptoms, Treatment, and
Preventions Tips. Disponível em:
www.steadyhealth.com/articles/Kidney_Cancer___Risks__Symptoms__Treatm
ent__and_Prevention_Tips_a918
[13] - www.biooncology.com/research-education/vegf/ligand
[14] - PAVON, L.S.; OKAMOTO, O.K. Aplicações de recursos
nanobiotecnológicos em câncer. Revendo Ciências Básicas, p. 74-77, 2007.
[15] – ELSAYED A. M.; Oral Delivery of Insulin: Novel Approaches, Chapter 11.](https://image.slidesharecdn.com/apresentao-drugdeliveryfinal-130806224430-phpapp02/85/Drug-Delivery-48-320.jpg)
