Produção de insulina recombinante
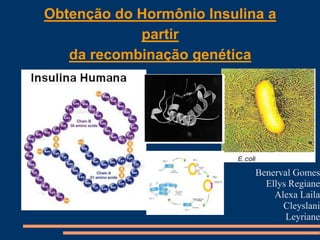
- 1. Obtenção do Hormônio Insulina a partir da recombinação genética Benerval Gomes Ellys Regiane Alexa Laila Cleyslani Leyriane
- 2. ● Em 2014, diabetes matou mais que HIV, malária e tuberculose somados. Fonte: https://noticias.uol.com.br/saude/ultimas-noticias/redacao/2015/09/17/em-2014- diabetes-matou-mais-que-hiv-malaria-e-tuberculose-somados.htm?cmpid=copiaecola
- 3. ● O Diabetes Mellitus é uma das doenças crônicas que mais avança entre a população mundial. A Federação Internacional do Diabetes estima que são cerca de 250 milhões de pessoas com o problema em todo o mundo – 4% delas (10 milhões) estão no Brasil. Segundo a Sociedade Brasileira de Diabetes, 33% da população brasileira dos 60 aos 79 anos de idade têm diabetes ou alguma alteração relacionada à glicose. Fonte: http://www.brasil.gov.br/saude/2012/04/diabetes
- 4. Os dois Tipos de Diabetes Mellitus: ● Tipo 1: em torno de oito por cento dos casos, que começa na infância e adolescência e não tem muita relação com a hereditariedade. Nesse caso, causa destruição das células produtoras de insulina ( hormônio sintetizado no pâncreas que promove a redução da taxa de glicose no sangue). ● Tipo 2: o mais comum, incidente em mais de 90% dos casos, tem relação significativa com a genética, com o envelhecimento, o excesso de peso e o sedentarismo. Nesta modalidade, existe uma resistência à ação da insulina no organismo. ● Fonte: http://bvsms.saude.gov.br/bvs/pu blicacoes/diabetes_mellitus.PDF
- 5. Função da Insulina no Organismo: ● A insulina exerce efeitos diversos sobre o metabolismo da maior parte dos diferentes tipos de alimentos – carboidratos, gorduras e proteínas. Sem a insulina um ser humano não consegue crescer, em parte por não poder utilizar mais que uma pequena porção dos carboidratos que ingere, mas também por suas células serem incapazes de sintetizar proteínas; ● Promove a entrada de glicose nas células; ● Regula a formação de ácidos-graxos no fígado, tendo função catabólica na oxidação de açúcares; ● Aumenta a velocidade no transporte de glicose para dentro das células musculares e do tecido adiposo.
- 6. Origem da Produção Industrial de Insulina: ● Desde o início da década de 1920, os pacientes diabéticos foram tratados com insulina, que foi purificada de pâncreas bovino ou suíno. ● O desenvolvimento no campo da engenharia genética permitiu a produção de insulina em E. coli e levedura, que foram aprovados para aplicações terapêuticas em humanos pela FDA. ● Hoje em dia, a insulina humana recombinante é produzida principalmente em E. coli ou Saccharomyces cerevisiae. ● Utilizando o sistema de expressão de E. coli, os precursores de insulina (IP) são produzidos como corpos de inclusão e polipéptidos totalmente funcionais são obtidos finalmente por procedimentos de solubilização e reenrolamento.
- 7. Continuação... ● A introdução da engenharia genética por Cohen e Boyer em 1973 estabeleceu o fundamento para a indústria biotecnológica atual, que se baseia na utilização de microorganismos ou culturas de células para a produção de proteínas que podem servir como produtos farmacêuticos, muitas vezes referidos como biofármacos. ● Alguns Anos mais tarde, os pesquisadores da Genentech clonaram os genes de insulina humano e de hormônio de crescimento e os expressaram em Escherichia coli, demonstrando a utilidade e aplicabilidade da engenharia genética na criação de bactérias geneticamente modificadas que produzem essas duas proteínas humanas.
- 8. Tecnologia de DNA Recobinante na produção de Biofármacos Alguns Biofarmacia produzidos por tecnologia recombinante: ● Insulina humana ● Hormônio de crescimento humano ● Fatores de coagulação do sangue humano ● Vacinas ● Anticorpos monoclonais ● Interferon ● Antibióticos e outros metabólitos secundários
- 10. Modificação celular de E. colli para produzir insulina humana: ● Uma das mais antigas produções tecnológicas recombinante de DNA; ● Realizado pela Genentech em 1978; ● Utilizava-se antes a insulina extraídas de pâncreas bovinos e suínos, mas induzia reações imunogênicas; ● Além disso, houve muitos problemas de purificação e contaminação; ● Para superar estes problemas, os pesquisadores inseriram genes de insulina humana em um vetor adequado (E.colli), que passou a expressar a proteína insulina semelhante a humana.
- 11. Vantagens de usar bactéria E.colli na produção de biofármacos: ●Muitas referências e experiências disponíveis; ●Ampla escolha de vetores de clonagem; ●Expressão gênica facilmente controlada; ●Crescer com altos rendimentos; ●Produto formado chega até 50% da proteína celular total; ●Pode ser concebido para a secreção em meios de crescimento permitindo a remoção de indesejados. Desvantagens: ● Nenhuma modificação pós-tradução; ● Atividade biológica e imunogenicidade podem diferir das proteínas naturais; ● Alto teor de endotoxina em gram negativos; ● O produto proteico expresso pode causar toxicidade celular; ● Organismos de inclusão difíceis de processar.
- 12. Como o processo de recombinação genética é feito em laboratório: ● Primeiro: em laboratório genes que codificam o hormônio insulina são inseridos nos vetores que são moléculas de DNA que se duplicam de maneira autônoma dentro de uma célula,carregando vários genes, entre os quais alguns marcadores que permitam reconhecer sua presença dentro da célula de E.colli. ● Segundo: o plasmídeo recombinante então são transferidos para células de E.colli. ● Terceiro: uma vez que os inóculos estiverem prontos são levadas ao meio de cultura em um balão de agitação para que se multipliquem. ● Quarta: o balão de agitação contendo o inóculo então é levado ao agitador de incubação onde pH e temperaturas são monitoras.
- 15. Processo de Bioprodução de Insulina Humana: Etapas: 1. Produção em Bancada ou Pequena Escala; 2. Escala piloto; 3. Biorreator (produção em larga escala); 4. Purificação 4.1. Clarificação/filtração/centrifugação 4.2.Concentração e/ou purificação de baixa resolução 4.3. Purificação de alta resolução 4.4.Operações para acondicionamento final do produto 5. Ajuste da potência e adição de excipientes 6. Filtração estéril enchimento asséptico 7. Envase.
- 16. 1. Produção em Bancada ou Pequena Escala ● Na grande maioria dos processos industriais de biofármacos, o desenvolvimento natural parte de uma escala de produção menor para uma escala maior. A variação de escala nesse sentido é conhecida como aumento de escala ou "scale-up". ● Caso contrário, ou seja, quando se está operando uma instalação industrial e se necessita elaborar ensaios em pequena escala, a fim de verificar certos aspectos tem-se a chamada redução de escala ou "scale-down". Fonte: BIOTECNOLOGIAINDUSTRIAL. VOLUME 11 ENGENHARIA BIOQUÍMICA
- 17. Continuação... ● Na escala de bancada, tendo em vista sua maior flexibilidade e menor custo de operação, os dados básicos sobre o processo devem ser levantados dentro do maior nível de detalhes possível. ● Nessa escala são realizadas tarefas básicas, como a seleção do microrganismo e o desenvolvimento do meio de cultura ideal. São também escolhidas as condições de temperatura e pH para o processo, assim como a forma de operação do biorreator. Fonte: BIOTECNOLOGIAINDUSTRIAL. VOLUME 11 ENGENHARIA BIOQUÍMICA
- 18. Continuação ….. ● Caso o processo seja aeróbio, deve-se conhecer a velocidade de consumo de oxigênio, a fim de que se possa dimensionar adequadamente o sistema de transferência de oxigênio. ● Ainda, esse levantamento de dados deve permitir a elaboração de modelos matemáticos, a fim de se poder visualizar o desempenho do processo em condições não pesquisadas experimentalmente, através da simulação do modelo, o que também auxilia o raciocínio nas etapas subseqüentes. Fonte: BIOTECNOLOGIAINDUSTRIAL. VOLUME 11 ENGENHARIA BIOQUÍMICA
- 19. Principais fatores a serem avaliados: ● Temperatura ( em torno de 37ºC) ● pH (em torno de 7) ● Crescimento Bacteriano; ● Taxa de Oxigênio Disponível; ● Composição do meio. Fases do crescimento bacteriano: Fase Lag: inóculo adapta-se ao meio; Fase Log: crescimento, início das divisões celulares; Fase Estacionária: fim do crescimento ou divisão celular; Fase de declínio.
- 20. Exemplo de aparelhos usados na produção de pequena escala. Ilustração de variação de escala.
- 21. Biorreatores típicos de cultura de células de bancada
- 22. 2. Escala Piloto: Operação é mais onerosa. Manter constante grande parte das variáveis do processo de bancada. Buscar operar na mesmas faixas: ● temperatura; ● pH; ● meio de cultura, etc.
- 24. 3. Biorreator: A Batelada ou Descontinuado
- 25. Sistema a Batelada ou descontínuo de produção: O fermentador é carregado com a matéria-prima e o inóculo correspondentes, a fermentação prossegue até o esgotamento dos nutrientes. Concluído o processo e extraído o produto, o fermentador é esvaziado, limpo e esterilizado antes de receber outra carga. A produção em bateladas é bastante utilizada na indústria farmacêutica porque o risco de contaminação permanece relativamente baixo.
- 26. Principais Componentes Presentes em um Biorreator a Batelada: 3.1 Meio de Cultivo; 3.2 Sensores; 3.3 Difusor de ar; 3.4 Chicanas ou quebra vortices; 3.5 Camisas ou serpentinas; 3.6 Agitadores (turbinas ou helices); 3.7 Filtros.
- 27. 3.1 Meio de Cultivo A composição do meio de cultura depende das necessidades metabólicas do microrganismo escolhido. Este deve conter todos os nutrientes necessários nas concentrações adequadas, que variam em função do microrganismo e do objetivo do processo. Composição básica: ●Água; ● Uma fonte de energia e de carbono: glicose (malaço de cana); ● Uma fonte de nitrogênio: inorgânica (sulfato de amônia, nitrato de potássio etc.), orgânica (asparagina, succinato de amônia, glutamato, ureia etc.) ou complexa (farinha de soja, peptona etc.); ● Sais minerais, tais como fosfato de potássio , sulfato de magnésio, cloreto de cálcio (CaCl2) etc; ● Elementos-traço: ferro, zinco, manganês, cobre, cobalto, molibdênio. ❏ Respiração aeróbia:C6H12O6 + 6 O2 +38 ADP + 38Pi 6 CO2 + 6 H2O + 38 ATP Glicose
- 28. 3.2 Sensores: Sensores fornecem sinais adequados, mesmo sob condições ambientais complexas, e que indiquem a evolução do processo. Principais sensores: Temperatura, Acidez (pH) e Oxigênio dissolvido (pO2) Temperatura: Devido à estrita dependência do crescimento microbiano para com a temperatura e pela facilidade de sua determinação, a temperatura é a variável mais frequentemente medida e controlada. •Temperatura ideal para o crescimento da E.colli se dá na em 37ºC Acidez (pH): Como a temperatura, o pH é frequentemente controlado nos processos biotecnológicos, devido à sua influência na atividade enzimática e no metabolismo microbiano. • O pH ideal para E.colli é na faixa de 7. Oxigênio Dissolvido (pO2): Como a solubilidade de oxigênio em meio líquido é baixa, o seu fornecimento ao meio, por transferência de massa, é de fundamental importância para evitar limitações ou controlar o desenvolvimento de processos bioquímicos.
- 30. 3.3 Difusor de ar: O suprimento de ar aos fermentadores é feito através de difusores ou dispersares de ar de vários tipos, sendo os de tubo aberto simples, em forma de Y ou anel de distribuição, colocados sempre abaixo da última turbina, os mais frequentemente utilizados. Os difusores de tubo aberto são os mais frequentemente utilizados em fermentadores agitados. Nesses casos, o tubo difusor deve ser preferivelmente afixado centralmente sob a turbina e o mais distante possível desta, a fim de reduzir o perigo de inundar a turbina em uma grande bolha de ar com a consequente queda na eficiência da transferência de oxigênio.
- 31. 3.4 Chicanas ou quebra vórtices A colocação de chicanas, quebra-vórtice ou "baffles" em fermentadores agitados mecanicamente é fundamental, para aumentar a turbulência e, por conseguinte, uma melhor oxigenação do meio.
- 32. 3.5 Camisas ou serpentinas; As camisas como as serpentinas podem ser internas como externas, neste caso sob a forma de semitubos, têm a finalidade de fornecer calor durante a esterilização como também retirar calor durante a fase de resfriamento e manutenção da temperatura de fermentação. Configurações de transferência de calor para biorreactores: (a) recipiente encamisado; (B) bobina externa; (C) bobina helicoidal interna
- 33. 3.6 Agitadores (turbinas ou helices) As funções do agitador ou agitadores em reatores de fermentação são múltiplas: homogeneização do meio, mistura da fase gasosa e aquosa, dispersão do ar, transferência de oxigênio e calor, suspensão de sólidos; enfim, manter as condições ambientais no meio de fermentação o mais uniforme possível. A turbina de disco com seis pás planas de Rushton é o tipo mais frequentemente utilizado.
- 35. 3.7 Filtros A esterilização do ar por filtração é, sem dúvida, a solução mais adequada para a obtenção de altas vazões de ar esterilizado, em virtude dos baixos custos envolvidos nesta operação, além de se dispor, presentemente, de filtros bastante confiáveis. Por esses motivos, a filtração é encontrada em praticamente todas as instalações industriais, tendo também dominado as aplicações em instalações de pequeno porte.
- 36. 4.PURIFICAÇÃO PURIFICAÇÃO 1. SEPARAÇÃO DE CÉLULAS E SEUS FRAGMENTOS DO MEIO DO CULTIVO 2. PURIFICAÇÃO DE BAIXA RESOLUÇÃO 3. PURIFICAÇÃO DE ALTA VELOCIDADE 4. OPERAÇÕES PARA ACONDICIONAR O PRODUTO CLARIFICAÇÃO/FILTRA- ÇÃO/CENTRIFUGAÇÃO ULTRAFILTRAÇÃO CROMATOGRAFIA DE TROCA IONICA E GEL FILTRAÇÃO CRISTALIZAÇÃO
- 37. 4.1. CLARIFICAÇÃO/FILTRAÇÃO/CENTRIFUGAÇÃO: Separação de células e seus fragmentos do meio de cultivo CLARIFICAÇÃO • A clarificação é a primeira etapa no processo de purificação; • Consiste na separação da célula do meio de cultivo.
- 38. CENTRIFUGAÇÃO: Células em suspensão de um meio líquido sofrem sedimentação por ação da força da gravidade (sedimentação); A centrifugação compreende a aceleração de sedimentação, por ação de um campo gravitacional centrífugo; Através da centrifugação resultam suspensões mais concentradas em relação à original; A centrifugação baseia-se na diferença de densidade entre a célula e o meio líquido, na viscosidade do meio líquido, na força motriz e no diâmetro da partícula; Na clarificação de microbianas, é utilizada centrifugas tubulares.
- 39. CENTRIFUGAÇÃO TUBULAR Podem operar sob refrigeração, mas possuem capacidade limitada de volume.
- 40. FILTRAÇÃO: Filtração Tangencial: Microfiltração Processos de microfiltração onde o fluido de alimentação escoa tangencialmente à superfície do meio filtrante; O fluxo filtrado e o coeficiente de retenção de solutos ou sólidos são influenciados pela formação de um gradiente de concentração de células ou solutos próximos à superfície da membrana e pelo “fouling”, que é o bloqueio ou estreitamento dos poros da membrana resultante da deposição de solutos no interior do meio filtrante.
- 41. TIPOS DE MEMBRANAS Membrana de fibra oca Possuem elevada área filtrante por unidade de filtro e são bastantes susceptíveis à entupimento
- 42. Membrana tipo placa e quadro Possuem pequenas áreas filtrantes por unidade de volume, são de fácil limpeza e podem ser aplicados em regime turbulento.
- 43. 4.2. Concentração e/ou purificação de baixa resolução Ultrafiltração: Compreende a separação da molécula alvo em relação a moléculas com características físico- químicas significativamente diferentes.
- 44. As moléculas com base no tamanho e forma. A amostra é colocada na câmara de ultrafiltração, onde fica diretamente acima da membrana de ultrafiltro. A membrana por sua vez assenta sobre um suporte macroporoso que lhe proporciona resistência mecânica. A pressão é então aplicada, fazendo assim com que moléculas maiores do que o diâmetro dos poros são retidos no lado a montante da membrana de ultrafiltro.
- 45. 4.3. Purificação de alta resolução • Compreende a separação de classes de moléculas com algumas características físico-químicas semelhantes; • Ela normalmente produz 98-99% de pureza. Emprego da combinação de duas técnicas cromatográficas. • CROMATÔGRAFIA IÔNICA • GEL FILTRAÇÃO
- 46. CROMATÔGRAFIA IÔNICA ➢ É a mais utilizada porque suas resinas empregadas apresentam elevada capacidade de adsorção de proteínas. ➢ É um processo de separação baseado na afinidade que componentes de uma amostra tem com os sítios iônicos em uma matriz sólida. A fase estacionaria, eletricamente carregada, tem a capacidade de reter solutos que estão na fase móvel e apresentam cargas de sinais opostos. ➢ Para ocorrer a adsorção de íons da fase móvel na estacionária, controlam-se fatores como pH e força iônica. Tem sua aplicabilidade muito ampla, já que todas as proteínas são eletricamente carregadas quando expostas a um determinado pH.
- 47. Gel filtração/Exclusão molecular: • Consiste na separação de biomoléculas de acordo com seu tamanho e forma. A coluna contém um polímero com ligações cruzadas com poros de tamanho definido. • As moléculas que são maiores migram mais rapidamente que os menores porque não conseguem penetrar no interior dos poros. • As moléculas menores, entram nos poros da coluna, levam mais tempo percorrendo, eluiem tardiamente em relação às maiores.
- 48. 4.4. Operações para acondicionamento final do produto ➢Cristalização
- 49. Cristalização: • Esse é um processo de agregação de cristais de moléculas presentes em soluções homogêneas supersaturadas. Faz a cristalização porque eles ficam estáveis, e assim as moléculas são imobilizadas. Formando assim cristais de insulina e adicionar os excipientes para a formação do liquido.
- 50. 5. Ajuste da potência e adição de excipientes SOLUÇÃO INJETAVEL DA INSULINA É adicionado os excipientes: ➢ Glicerol: Solvente ➢ Metacresol ➢ Fosfato de sódio dibásico di-hidratado: fosfato de sódio dibásico di-hidratado ➢ hidróxido de sódio: Agente alcalinizante ➢ ácido clorídrico (ajuste de pH): agente acidificante ➢ Água para injetáveis
- 51. 6. Filtração estéril enchimento asséptico Representação fotográfica de uma máquina de sopro- enchimento-selagem, que pode ser particularmente útil no enchimento asséptico de produtos líquidos
- 52. 7. Envase
- 53. ➢Milhares de vasilhames serão cheios com a insulina pronta para o consumo humano. As insulinas serão colocadas em tubos que serão usados nas canetas, para facilitar a sua aplicação.
- 54. ➢ O enchimento do produto nos recipientes do produto final é realizado dentro da zona do grau A. O processo de enchimento é altamente automatizado, não necessitando de contato direto entre o operador e o produto. Isso minimiza As possibilidades de contaminação acidental do produto pelo pessoal de produção. ➢ A insulina pode ser embalada e mantida refrigerada por meses. Isso faz que haja um estoque para manter a produção.
- 55. ➢ As canetas de aplicação da insulina Todo o processo do enchimento dos vasilhames são feitos por máquinas. As diferentes partes das canetas são despejadas em três torres diferentes, que posicionam as peças automaticamente. As canetas com insulinas são montadas desta forma: Dosador na parte debaixo com os números Acima o recipiente com o injetor que libera a insulina, Na parte de cima da caneta é encaixada a agulha
- 56. ➢ Para a produção da insulina pura, até ela sair da fábrica empacotada, leva em média 7 meses, mas pode chegar a 9 meses ou mais.. A produção sem interrupções garante o abastecimento constante. ➢ Como leva um grande tempo para poder fabricar a insulina, são feitos controles e inspeções por funcionários constantemente, para que tenha o mínimo de perda possível. ➢ O controle de qualidade pega uma pequena parte de cada etapa feita, para saber se está dentro do esperado. ➢ Apesar dos processos de fabricação da canetas serem todos automatizados, os engenheiros fiscalizam cada etapa também.
- 57. Bibliografia: